用于确定生物系统的质量和/或机械特性的测量装置和方法与流程
当前技术中已知用于确定生物系统的质量和/或机械特性的测量装置。
在Park K、Jang J、Irimia D、Sturgis J、Lee J、Robinson JP、Toner M、Bashir R.的Living cantilever arrays for characterization of mass of single live cells in fluids.,Lab on a Chip.8:1034-41(2008)(“用于表征流体中的单个活细胞的质量的活性悬臂阵列”)中,开发了悬臂阵列来确定溶液中的细胞的质量。这些阵列通过两组彼此对置的悬臂形成。外部正弦电源以180°相移连接到对置的悬臂组,以便生成不均匀电场,不均匀电场通过介电泳捕捉细胞。没有有效的激励方法使悬臂振荡。悬臂仅仅由于热噪声而振动,这样会降低这个装置测量质量变化的敏感性和时间分辨率。在开始质量测量之前,需要几天(通常三天)让细胞在悬臂上生长。这意味着选择随机细胞进行实验。由于这个装置的设计,它的使用无法与用于生物学的现代的光学显微技术(例如微分干涉差(DIC)、荧光、共聚焦或相衬显微技术)兼容。这些技术在生物学中是非常重要的,因为它们提供了关于所表征的细胞或生物系统的额外形态和功能信息。
Park K、Millet LJ、Kim N、Li H、Jin X、Popescu G、Aluru NR、Hsia KJ、Bashir R.的研究Measurement of adherent cell mass and growth.PNAS,107:20691-6(2010)(“粘附细胞质量和生长的测量”)显示了一种使用微型隔膜谐振器确定流体中的单个粘附细胞的质量和机械特性的装置。使用洛仑兹力使隔膜有效地受到激励。为了执行此操作,将隔膜浸没到均匀磁场中,交流电流流过隔膜。通过使用激光多普勒干涉仪(LDI)检测到隔膜的移动。为了将细胞附着到隔膜,在装置上培养细胞。这样做,一些细胞将随机附着到隔膜的顶部。一旦细胞被注射到装置中,在开始测量之前需要至少两个小时的等待时间,这样会显著限制有待研究的细胞过程。这个系统与荧光兼容,但是无法与DIC或相衬显微技术兼容。
S.Son、A.Tzur、Y.Weng、P.Jorgensen、J.Kim、M.W.Kirschner、S.R.Manalis.的Direct observation of mammalian cell growth and size regulation.Nat.Methods.9:910-2(2012)(“哺乳动物细胞生长和大小调节的直接观察”)中的装置是基于微型通道谐振器,这是一个被真空包围的中空悬臂。漂浮在流体中的悬浮细胞可以被泵吸到悬臂中并且通过悬臂。当细胞经过悬臂的自由端时,细胞的漂浮质量会使悬臂的总质量增加,这样会降低悬臂的谐振频率。此外,只能对穿过单独的储集器的细胞而不是在细胞通过质量传感器时执行高分辨率荧光显微技术。这个工具并不适合于粘附细胞,因为该细胞必须悬浮才能够漂浮通过悬臂。此外,无法研究一些细胞过程,因为该装置只能检测到漂浮质量。这种检验的另一个不利问题是,既无法长时间(>>1秒)也无法同时持续地采集单个细胞的荧光信号(例如显微技术)和漂浮质量,从而导致很难使漂浮质量与细胞状态相关。
本发明的目标是改善这些已知装置。
根据本发明的第一方面,通过提供一种用于确定生物系统的质量和/或机械特性的测量装置来实现这个技术难题的解决方案,该测量装置包括微型悬臂和激励悬臂的强度经过调制的光源,优选的是激光,其中该悬臂经过功能化(functionalized)以附着到生物系统。该测量装置允许随时间并且在生理上相关的环境中确定例如单个细胞或小组织的生物系统的质量和/或机械特性。此外,该测量装置可用于研究细胞与细胞或者细胞与组织的相互作用。
“生物系统”是例如一个细胞、细胞群组或小组织。细胞可以是粘附的或非粘附的并且有各种来源,例如人、动物、酵母和细菌。
“光源”是任何能够生成具有优选地但不限于350nm到750nm的范围的波长的电磁信号的装置。该电磁信号可以是相干的或不相干的,单色的或者非单色的。
为了附着例如细胞之类的生物系统,使悬臂功能化。悬臂的功能化可能意味着,悬臂被物理地或化学地改变以便展现不同的物理、化学或生物特性。功能化可以具有不同于例如将生物样本附着到悬臂或诱发样本的特殊表现的应用。作为悬臂的化学功能化的替代方案,其它将生物系统附着到悬臂的方法也是可能的。具体来说,可使用微型通道悬臂,其借助于抽吸机制将生物系统附着到悬臂。偶尔的情况下,如果因为样本与悬臂之间已经存在物理或化学相互作用,所以生物系统无需特定的结合方式就能附着到悬臂,则特定的功能化将不是必需的。这些替代方案将被所属领域的技术人员视为等效于化学功能化。
可以通过使单个细胞(或细胞群组)直接接触悬臂而将其附着到悬臂。测量系统可以从培养的细胞群体中选择和拾取某一细胞,由此允许针对性地测量所选细胞的质量和/或机械特性。此外,非粘附细胞的测量也是可能的,因为它们可以固定在悬臂的末端。这样允许在非常的时间段中进行测量,因为测量可以在细胞被拾取后立刻开始。因而测量可能通常在几秒或最多几分钟时间内开始。测量装置能够直接测量总质量,因为附着到悬臂的生物系统会将它的所有质量添加到悬臂的质量,从而改变悬臂的谐振频率。此外,通过与我们的装置兼容的光学方法,例如SLIM(空间光干涉显微技术),可以检测到生物样本的干质量。直接检测细胞的总质量的可能性对于理解细胞周期调节或其中细胞可以摄取或释放水的任何其它过程是至关重要的。重要的是应注意,其它当前技术系统不能检测单个细胞的总质量,只能检测其漂浮质量。通过测量在两种不同密度的流体中的单个细胞的漂浮质量并假设细胞的体积和质量在这些条件下保持不变(情况可能并不是这样),那些系统可能试图估计总质量。然而,每次测量时都要改变细胞存活介质,这样的要求可能对细胞的压力巨大,而且肯定与生理条件相差很大。
它还可以用于研究细胞的机械特性,例如粘附力、刚度或流变特性。细胞相对于某一基质或另一细胞的粘附力可以这样测量:首先将细胞固定在悬臂上,然后使得这个细胞在特定的时间量中接触基质或细胞。在前一时间之后,系统从基质或细胞上收回悬臂上的细胞,并且通过测量悬臂的偏转量来测量该过程所必需的力。细胞的刚度可以通过如下方式测量:将细胞限制在悬臂与基质之间,然后在用控制的方式改变悬臂的底部与基质之间的距离的同时分析悬臂的偏转量。还可以通过将细胞附着在悬臂上并且在远离基质的位置(通常数十微米或更大)设立悬臂来确定细胞的刚度。在这些条件下,悬臂以谐振频率振荡,并且它的品质因数的改变可以与细胞的刚度的改变相关。但是,还可以应用其它提取机械特性的可能性。此外,测量装置能够使得单一细胞接触或接近另一细胞或组织,以便研究细胞和组织之间的细胞相互作用。
测量装置使用悬臂的光热激励原理,由此允许测量装置提高质量敏感性和时间分辨率。为了直接激励悬臂而不激励装置的任何其它部分(其它部分可能会引入噪声),将强度经过调制的光源,优选的是激光,选址(addressed)在悬臂上。这个激光产生非常局部化的、经过调制的加热,其相应地激励悬臂。激光可以被数字和/或模拟地调制。悬臂是吸收性的,即对于光源的波长也是部分地吸收性的。悬臂的材料可以是硅,但是也可以使用具有类似特性的其它材料。悬臂不需要有待用激光激励的任何涂层,但是它也可以完全地或部分地涂布有金属。优选的是,有待放置生物样本的区域上不涂布金属。
为了提高质量敏感性,悬臂的经过功能化的侧面可以安置成靠近微型悬臂的自由端。因此,悬臂可以完全或部分地功能化。
生物系统的质量和/或机械特性的检测来自悬臂的驱动移动的分析。悬臂的谐振频率是悬臂的质量的函数。当生物样本附着到悬臂时,悬臂的质量改变,这样使得其谐振频率改变。基于悬臂和附着的生物样本来检查系统的谐振频率,从而追踪生物样本的质量变化。根据未附着样本的悬臂与附着了样本的悬臂的谐振频率之间的比较,可以获得附着样本的质量。此外,测量装置能够评估转移到悬臂的能量消耗得有多块,这是被称作品质因数或Q-因数(Q-factor)的无量纲量值的测量。量值、谐振频率和Q-因数都可能受到附着到悬臂的样本的机械特性的影响,这样也允许装置对于那些变化敏感。此外,使用额外参数来提取信息是可能的,例如,悬臂移动的相位(激励信号和悬臂响应之间的延迟)和振幅。
用于读出悬臂移动的系统不像悬臂激励方法那样至关重要,并且可以使用多种系统完成,例如:射束偏转、压电电阻性检测、多普勒干涉测量法等等。这个系统允许对于每个频率获得悬臂移动的两个主量值:振幅和相位。振幅是给定频率下悬臂的最大伸长率;相位与悬臂相对于激励信号的响应延迟有关。获得的信息的相应计算导致所期望的质量和/或机械特性的确定。
有利的是,将悬臂完全浸没在缓冲溶液中。这样允许在生理条件下检测生物系统的总质量。可使用流体细胞。
本发明的第二并且有独立发明性的方面涉及一种用于确定生物系统的质量和/或机械特性的测量装置,其包括微型悬臂和激励悬臂的强度经过调制的光源,优选的是激光,其中悬臂对可见光谱的波长是可透射的(transparent)。悬臂对可见光谱的波长可以是部分地或全部地可透射的。有利的是,生物样本将要放置的区域对可见光谱的某一波长是至少部分地可透射的。这样允许将质量和/或机械特性的确定与细胞生物学中的重要光学技术组合。
优选地,悬臂的靠近其自由端的并且对可见光谱的至少一些波长部分地可透射的部分不小于10μm×10μm。针对可见光谱的至少一些波长的透射性(transparency)或部分透射性的这个窗口是装置与例如DIC(微分干涉差)或等效技术之类技术兼容的一项要求,这类技术允许获得关于生物样本的形态的关键信息。这些类型的技术需要特殊类型的照明,其必须通过样本并且使用位于照明光源相对位置的特殊光学显微镜收集,如图2中可以看出。除了DIC信息之外,图2中所示的物镜还允许我们的装置从样本获得荧光信息。但是,悬臂的透射性或部分透射性并不是针对荧光信息的要求,因为激励样本的荧光的照明可以通过物镜而被驱动,物镜同时收集从样本发射的荧光。
本发明的第三并且具有独立发明性的方面涉及一种测量装置,其中该测量装置用于确定生物系统的质量和/或机械特性,该测量装置包括微型悬臂和激励悬臂的强度经过调制的光源,优选的是激光,该测量装置包括光学显微镜,具体来说是荧光显微镜、共聚焦显微镜、荧光能量转移(FRET)显微镜、DIC和/或相衬显微镜,所有这些显微镜具体来说作为倒置显微镜。细胞生物学中的光学技术与质量和/或机械特性测量的这种组合,允许更好地理解质量测量,因为可以观察到细胞的形态。这样允许测量装置检测细胞质量并且使这个信息与细胞状态和形状相关。
虽然存在通过光热激励使悬臂振荡的原子力显微镜(AFM),但是那些系统不与例如DIC、荧光显微技术等现代光学技术兼容。典型的原因是,总的来说,那些AFM系统使用光学显微镜将强度经过调制的激光聚焦在悬臂上,以便激励(振荡)悬臂,这样会消除使用显微镜进行荧光成像的可能性。相反,本文所述的装置被设计成使得强度经过调制的激光可以使用特殊的一组光学元件和纳米定位器(见图3)定位并且聚焦在悬臂上。光学路径允许从装置的顶部和底部的光学通路(optical access),而不会连累悬臂激励机制。另外,反过来说也成立,也就是,悬臂激励不会连累现代光学技术的信息采集,这两种类型的系统能够同时工作。这个事实连同悬臂、悬臂支座和样品支座的透射性,使得该装置与现代光学技术完全兼容。重要的是应注意,所描述的装置与用于近场光学的系统共享一些特征,但是存在重大差别。举例来说,一些用于近场光学的系统具有悬臂以及附着到悬臂的波导。激光聚焦在波导上,波导必须非常靠近含有金属的样本(通常几纳米或几十纳米),以便激励等离子。本文所述的装置不具有附着到悬臂的波导。此外,本文所述的装置不使用激光来诱发近场光学的效应,例如等离子的激励,而是使悬臂随时间偏转。此外,本文所述的装置能在样本无需含有金属的情况下从其中提取信息。这个装置中的样本附着到悬臂。在确定样本的总质量的同时,悬臂(样本附着到悬臂)的位置远离培养生物样本的皮氏培养皿(petri dish)或容器的表面,以避免可能的相互作用而影响测量。当操作在圆化时可具有大约10-20微米的直径的哺乳动物细胞时,含有细胞的悬臂与皮氏培养皿的表面之间的距离通常是数十或数百微米。此外,本文所述的装置利用第二激光器,其位置靠近悬臂的自由端以便读出悬臂的偏转量。然而,这个第二激光器并不是必须的,可以应用其它系统,例如压电悬臂、压阻式悬臂、多普勒干涉计等。
该测量装置允许以高时间分辨率并且以非侵入性方式量化在细胞周期中转变的单个细胞的质量和/或机械特性,其方式是通过允许将细胞质量与细胞相位和形状持续相关。此外,可以定制质量传感器以研究单个细胞或小型细胞群体。
优选的是悬臂的长度处于10μm到1000μm的范围内。例如在测量直径大约20μm的细胞的情况下,悬臂的长度可以是大约75μm。此外,悬臂具有谐振频率,优选的是处于1Hz到10MHz范围内,优选的是处于20kHz到1200kHz范围内,优选的是在悬臂浸没在水中时处于20kHz到400kHz范围内。在谐振频率的此范围内,系统可以被调适成测量直径大约1-30微米的单一细胞,但是也可以测量更小或更大的生物系统。最后,悬臂具有振荡振幅,优选的是处于0.01nm到300nm范围内,优选的是小于30nm。为了优化测量装置,可以通过针对不同应用调适悬臂尺寸,根据将测量的目标生物系统来选择或调适悬臂。
优选的是光源可以是波长处于从350nm到750nm的范围内的激光。其波长可以在350nm与550nm之间,优选的是在350nm与450nm之间。具体来说,可使用405nm的波长,这具有额外优点,即它足够远离荧光显微技术中使用的许多波长。然而,根据悬臂材料,也可以使用其它波长。具体来说,激励激光的波长被选择而使得它被悬臂强烈吸收。有利的是,悬臂上的激光点的位置、直径和焦点可以经过调整并且可以位于悬臂的底部处。这样会使激励效率最大化。激光点的直径可以小于100μm,优选的是小于30μm,优选的是小于10μm。这个大小允许高效地激励悬臂并且同时允许激光远离生物系统以避免与样本相互作用。为了增加质量敏感性,生物样本通常定位成靠近悬臂的自由端。
另外并且有利的是,微型悬臂和功能化侧面上的光源(优选的是激光)点可以位于悬臂的相对面上,生物系统附着于功能化侧面上,以防对有待研究的细胞造成任何影响。
本发明的第四方面涉及一种用于确定生物系统的质量和/或机械特性的方法,其包括以下步骤:
a.确定悬臂的弹性常数
b.用某一频率的光源优选的是激光激励悬臂,
c.在附着生物系统之前测量悬臂的谐振频率和/或悬臂移动的振幅和相位
d.使悬臂接近样品支座内的所选生物系统
e.将生物系统附着到悬臂,
f.测量悬臂的谐振频率和/或悬臂移动的振幅和相位以与在步骤c)中获得的谐振频率和/或振幅和相位比较,以及
g.计算生物系统的质量和/或机械特性。
必要时,悬臂的功能化可能在步骤a)之前或之后。替代地,步骤a)可以在步骤f)之后执行。在这种情况下,在执行步骤a)之前必须清洁悬臂以移除样本的任何残留。在步骤中e)将生物系统结合到表面的情况下,可以使悬臂接近样本以拾取样本,然后离开表面,使样本保持附着到悬臂,以避免该表面对悬臂的谐振频率造成可能的影响。在远离样本安放表面的位置可以执行步骤f)。即使在实验之后也可以进行步骤f),因为这意味着只有计算。通常100-200μm就够远了。还在足够远离表面的位置进行步骤c)以避免该表面对测量造成可能的影响。
另外,可以在悬臂未缩回的情况下执行测量。然而,在这种情况下悬臂不能自由振荡并且必须相应地解释所获得的信息。
通过频谱的扫掠过程允许通过映射悬臂的移动(即观察振幅和相位)来确定谐振频率。
这种测量方法允许对细胞进行针对性选择并且对质量和/或机械特性进行特定测量。具体来说,有可能不仅测量单个细胞的漂浮质量而且测量单个细胞的总质量。因此,微型悬臂可以完全浸没在缓冲溶液中。
在步骤a)中确定悬臂的弹性常数可以按如下方式执行
a'用某一频率的激光激励悬臂,
b'确定悬臂的谐振频率。
这样允许校准悬臂弹性常数,由此允许测量总质量。使用激光的有效激励来确定谐振频率的过程是非常准确的。这个过程通常在空气环境条件下进行,它的目标是找到悬臂的弹性常数。一种非常准确的方式是通过使用赛德法(Sader's method)。为此,使用强度经过调制的激光激励悬臂以扫描足以找到悬臂的谐振频率的频率区间。根据频率扫描确定悬臂的谐振频率和品质因数。使用该信息连同空气密度和悬臂的尺寸和材料,可以推导出悬臂的弹性常数。但是,还可以利用其它方法,例如基于悬臂在空气环境条件中或在液体中的热噪声的测量,或者通过分析在用已知弹性常数的另一悬臂按压时悬臂的弯曲。当确定悬臂的谐振频率时,悬臂应当远离样品支座的底部以避免受到样品支座的表面的影响(通常100-200μm就够远了)。
然而,还可能基于热能振动使用校准程序来确定悬臂的谐振频率,但是准确度可能要低很多。因为热能,其与悬臂的温度相关,悬臂以极小的振幅在谐振频率下振动。在一些情况下,这个振幅太小,以至于可能很难检测到。使用例如频谱分析器,可以分析悬臂的这个移动并且测量其谐振频率。这种方法不需要有效地激励悬臂,当悬臂浸没在液体中时,难以有效地激励悬臂。可以按照建议通过使用强度经过调制的激光来解决这个问题,强度经过调制的激光引起悬臂非常彻底的激励和响应。
该测量方法可进一步包括在步骤a)之前执行的下面的额外步骤
a”选择生物系统,
b”使悬臂尺寸适应所选的生物系统。
使悬臂适合生物系统,这增加了测量值的分辨率,即,使悬臂的大小适应细胞类型和例如其大小和/或质量。
一种使悬臂适应生物系统的方式是通过使用聚焦离子束切下一片硅,例如由硅制成的大悬臂。这种技术允许消融具有非常高的分辨率的材料,但是所属领域的技术人员已知的其它方法和技术可以同样被应用来制造悬臂。
此外,可在步骤f)中使用反馈回路以高时间分辨率追踪生物样本随时间的质量变化。使用一个或几个反馈回路增加敏感性和时间分辨率。具体来说,可使用锁相回路(PLL)。其中悬臂的相位用作控制变量,而调制激光强度的信号的频率用作被控变量。控制条件是找到激励信号的产生π/2的悬臂相位的频率。使用这种系统,可以自动追踪悬臂的谐振频率,因此可以直接测量质量变化。
此外,可独立地或累积地使用第二反馈来获得关于有待研究的生物系统的另外的信息。这个反馈使用悬臂的振荡振幅作为控制变量,而使用用于调制激光强度的信号的振幅作为被控变量。因此,确保悬臂的振幅在较长时间保持不变。这样做,可以获得系统的减振的相关信息。
可使用悬臂的基础挠曲模态或更高的挠曲模态。
附图说明
下文中将参照示例性实施例更详细地描述本发明。在图中,
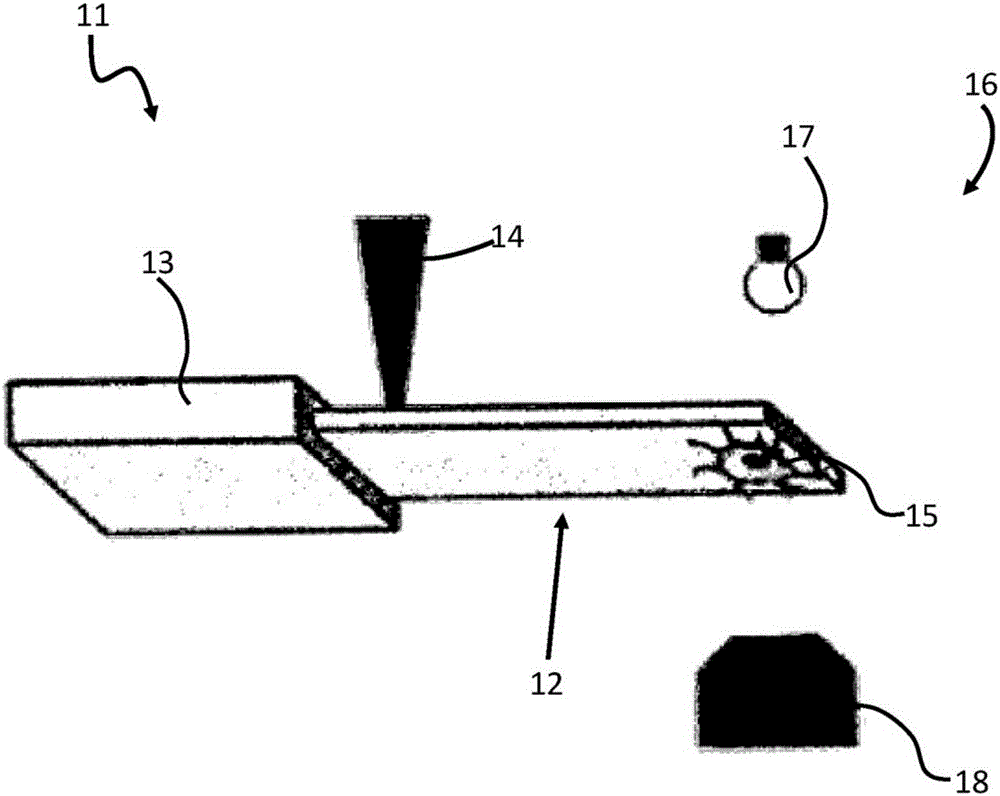
图1示出了测量装置的示意性表示,
图2示出了具有光学显微镜的测量装置的示意性表示,
图3示出了具有光学显微镜的测量装置的更高详细级的示意性表示,
图4示出了测量装置的二维俯视图,用箭头指示移动方向,
图5示出了测量装置的二维俯视图,
图6示出了测量装置的二维仰视图,
图7示出了测量装置的二维横截面图,
图8示出了第一视角中的测量装置的三维俯视图,
图9示出了第二视角中的测量装置的三维俯视图,
图10示出了测量装置的三维仰视图,
图11示出了第一视角中的三维横截面图,并且
图12示出了第二视角中的三维横截面图。
图1中的测量装置1具有位于固定件3中的悬臂2。悬臂2受到强度经过调制的激励激光4的激励。这样允许通过聚焦在悬臂2上的强度经过调制的激光4直接激励悬臂2。激光4产生非常局部化的经过调制的加热,其激励悬臂2。这个激光点的位置、直径和焦点可以经过调整,并且这个激光点通常位于悬臂2的底部处以使激励效率最大化。生物系统5通常安置成靠近微型悬臂2的自由端以增加质量敏感性。另外,为了防止对有待研究的生物系统造成任何影响,激励激光4和生物系统5(例如一个细胞或几个细胞)优选地并且有利地位于悬臂2的相对面上。因此,悬臂2的功能化侧面放置成靠近这个自由端。这整个布置可以放置在流体细胞内。
根据图2的测量装置11包括在固定件13中的悬臂12,悬臂12受到悬臂12的底部处的强度经过调制的激光的激励。这里同样,生物样本15通过功能化被结合到悬臂12的自由端。另外通过光源17和透镜系统18构成的光学显微镜16设置测量装置11。所使用的显微镜16是倒置显微镜。
如图3中所示的测量装置20将用于确定生物系统的质量和/或机械特性的测量装置与细胞生物学中的光学技术组合。DIC或相衬照明21与倒置显微镜34一起形成测量装置的相应光学部分。
对于测量装置的确定生物系统的质量和/或机械特性的部分,强度经过调制的激光22发射波长例如405nm的激光束,其通过双色镜25聚焦并且反射在悬臂上,双色镜25选择性地反射激光的波长,例如405nm。通过改变激光焦点的位置可以修改悬臂37上的激光点直径。
悬臂支座32固持悬臂37。具有激光23的第二光学路径读取悬臂37的移动。这个激光23例如以850nm的波长工作。这个第二激光(连续线)的激光束通过长度系统26聚焦在悬臂上,并且通过双色镜24被引导到悬臂,双色镜24选择性地反射第二激光23的波长,例如850nm。在悬臂处反射激光束之后,光束被镜面31再次重定向通过带通滤光片35,在光束命中光电二极管36之前,带通滤光片以相应波长(例如850nm)为中心,这样允许通过检测激光束的移动来检测悬臂的移动。为了持续追踪生物样本的质量和/或机械特性,自动致动镜面31和光电二极管36,从而确保被反射的光束23将随时间在中心处命中光电二极管。这个自动化可能非常重要,因为生物样本可能随时间使悬臂弯曲,从而将激光抽离光电二极管的中心。在被反射的光束的方向上校正不会扰乱对悬臂的谐振频率的追踪。为了容许悬臂37相对于样本(未图示)移动,即为了让装置用悬臂37拾取处于样品支座33(例如皮氏培养皿)上的某一样本,用类似致动器28的致动器在竖直方向中移动悬臂。另外,平台29配备有两个XY定位器以移动用于设备27和样品支座33的盒子。
图5到图8中针对一个实施例示出的测量装置40将用于确定生物系统的质量和/或机械特性的测量装置与细胞生物学中的光学技术组合。然而,这里未示出光学显微镜。也未示出测量装置的固持样本的下部部分。
图4到图12中所示的测量装置的上部部分允许确定生物系统的质量和/或机械特性。为激励悬臂60而设置第一光学路径。强度经过调制的激光(未图示)在405nm的波长下发射激光束56。这个激光束56通过光学系统55进入测量装置40,光学系统55聚焦405nm的激光束。这个光学系统55通过两个定位器系统固持,即第一定位器系统50和第二定位器系统51。第一定位器系统50固持光学系统55以聚焦405nm的激光束56。第一定位器系统50可以如图4中的箭头所示移动,这例如允许改变悬臂60上的激光点直径。第二定位器系统51固持第一定位器系统50和双色镜49。双色镜49反射405nm的波长,从而允许可见光谱中的其它波长和850波长通过。这个第二定位器系统51可以如图4中的箭头所示移动,这允许定位405nm的激光束56而使其命中某一位置,例如悬臂60。系统40的这个追随激光束56的第一光学路径由此确保能量从强度经过调制的激光(未图示)到悬臂60的可调节的转移。悬臂60本身通过悬臂支座62得到固持。
跟随具有850nm波长的激光束44的第二光学路径读出悬臂60的移动。这个第二激光束54通过光学系统53进入测量装置以聚焦850nm的激光束54。光学系统53通过两个定位器系统固持,即第一定位器系统45和第二定位器系统46。定位器系统45固持光学系统43以聚焦850nm的激光束54。这个定位器系统45可以如图4中的箭头所示移动。这样允许例如改变悬臂60上的激光点直径。第二定位器系统46固持第一定位器系统45和双色镜47。双色镜反射850nm波长,从而允许可见光谱中的其它波长通过。并且,这个第二定位器系统46可以如图4中的箭头所示移动。这样允许定位850nm激光束54而使其命中某一位置,例如悬臂60。通过悬臂60对850nm激光束的反射,允许这个光学路径读出悬臂60的移动,通过镜面57继续使850nm激光束朝向光电二极管59选址。四象限光电二极管59允许通过检测850nm的激光束54的位置而读出悬臂60的移动。镜面57可以旋转以允许在光电二极管59上定位850nm的激光束54。因此,致动器43通过使镜面的支座旋转而移动镜面57。另外,定位器系统48允许如图4中的箭头所示移动光电二极管59。这个系统例如可以结合致动器43使用以使850nm的激光54命中光电二极管59的某一部分。此外,这个第二光学路径含有带通滤光器58,其以850nm的波长为中心。这个带通滤光器58避免非常不同于850nm的其它波长到达光电二极管59,从而增加光电二极管59的信噪比以限定(dictate)850nm的光并且避免由系统中的其它波长导致检测中的可能干扰。
该窗口44允许通过提供DIC、相衬或其它照明类型的充分接近而与光学技术组合。
放置在盒子的底部41上以固持设备的整个系统可以通过致动器42、42'和42”移动,该致动器允许移动盒子且因此沿着竖直方向移动悬臂。这些致动器42、42'和42”例如允许使悬臂60接近和离开样本(未图示)。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于控制、检测、调节和/或分析生物、生物化学、化学和/或物理过程的系统、方法、计算机程序产品和用户接口与流程
- 用于移动健康系统中的用户识别的生物辨识的利记博彩app与工艺
- 一种用于豌豆化肥的多种微生物添加设备及使用方法与流程
- 用于确定生物系统的质量和/或机械特性的测量装置和方法与流程
- 用于稳定和维持顽强微生物的生存力的组合物和方法与流程
- 用于从微生物生物质中回收脂质的方法与流程
- 用于生物材料和微生物的保存和保护的糖肽衍生物的利记博彩app与工艺
- 用于充气食品的粉末组合物的利记博彩app与工艺
- 一种用于微生物法定量检测维生素B12的微孔板、其试剂盒及其制备方法与流程
- 一种用于有机物的微生物分解工艺的智能控制方法及其系统与流程
- 一种用于室温H2S气敏传感材料氧化镍及其制备方法与流程
- 一种用于检测UO22+的液晶生物传感方法与流程
- 一种用于3D打印的生物墨水材料及其制备方法和应用与流程
- 用于智能传感家庭的设备、方法、以及相关的信息处理与流程
- 一种楼宇室内信号覆盖用RFID传感馈线的利记博彩app与工艺
- 一种用于救援的传感网络抗失效定位切换控制方法及系统与流程
- 用于集成型工业机械传感控制的旋转编码器的利记博彩app与工艺
- 用于控制、检测、调节和/或分析生物、生物化学、化学和/或物理过程的系统、方法、计算机程序产品和用户接口与流程
- 一种用于MIMO‑SCMA系统的信号似然比计算方法及装置与流程
- 生理信号采集传感带及其应用的利记博彩app与工艺