一种双金属银铜纳米颗粒及其应用的利记博彩app
本发明属于化学
技术领域:
,具体涉及一种双金属银铜纳米颗粒及其应用。
背景技术:
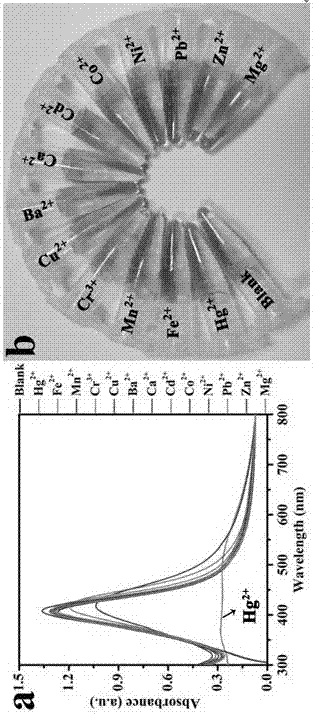
:现代工业的快速发展和人类对资源的掠夺性开采导致重金属引起的水体环境污染严重。因此,实现对污染水体中重金属离子的快速灵敏检测和硝基酚类化合物的快速催化降解具有重要的研究意义。重金属污染已成为世界比较重要的环境污染之一,重金属,原定义是指比重在4.5g/cm3的金属,大致有54种位于重金属元素行列,具体如汞、铜、铅、镉、铬、锰、镍、钴和锌等。尽管某些重金属元素如铜、锰、锌等是人类生命活动所必需的微量元素,但同其他大部分非生命活动所必须的重金属元素一样,当其在体内含量超过一定浓度时会对身体造成巨大的危害。汞是环境中普遍存在的高毒性、对人类健康有极大影响的有害物质。汞在污染水体中主要以hg2+形式存在,是各种形式的汞污染物质中的最普遍且最稳定的一种。在1953年出现在日本并震惊世界的“水俣病”正是由于汞污染引起的。当人体摄入过量的hg2+时,神经系统会受到严重损伤,导致运动失调、头痛头晕,并且对肝脏和肾脏等造成严重损伤。对于人类活动造成的环境水体污染,主要为电池、氯碱、电子和塑料等工业废水的排放及某些废旧医疗器械处理不规范造成生态环境水体的污染。所以能够精确灵敏的检测重金属离子(hg2+)对社会环境与国家安全来说是非常有意义的。硝基酚类化合物是一类重要且常用的化工原料,作为原材料或中间体被广泛应用于炸药、医药、杀虫剂、染料、木材防腐剂和橡胶等生产中。硝基酚类化合物在生产和使用过程中,会随工业废水的排放对环境造成污染。铁氰化钾(k3fe(cn)6)能分解出毒性很强的氢氰酸,会对环境造成污染。因此找到高效的催化剂催化降解硝基酚类化合物和铁氰化钾至关重要。双金属纳米粒子由于具有较高的光学、催化、磁性以及电学性能已被广泛应用在各种领域,如比色传感器、催化剂、燃料电池的制造和抑菌作用。双金属纳米颗粒结构的优势与其形态(大小、形状等),微观结构(合金化、核壳等)和电子结构(电荷转移、轨道杂化等)有一定的联系,从而产生促进和可调谐性的物理和化学性质。双金属纳米颗粒可以同时或连续加入合成的前驱体形成合金或金属核壳结构,而且双金属纳米颗粒在一般情况下能够提高催化性能相比于单金属纳米颗粒,此方法是采用水相氧化还原法以硼氢化钠作为还原剂合成双金属银铜纳米颗粒。技术实现要素:本发明的目的是提供一种双金属银铜纳米颗粒制备方法及其比色探针的检测应用。一种双金属银铜纳米颗粒ag-cunps溶液,它是由下述方法制备的:在磁力搅拌下,向装有10-30ml超纯水的烧瓶中加入0.1m的硫酸铜50μl和0.1m的柠檬酸钠50μl的混合溶液,之后迅速加入新配制的0.5-1.5ml的硼氢化钠溶液;15min后,加入0.1m的硝酸银溶液50μl,继续磁力搅拌10-30min;所述的硼氢化钠溶液为:3.8mg硼氢化钠加入4ml超纯水;所述的硼氢化钠溶液添加量为1ml;所述的磁力搅拌时间为20min。一种双金属银铜纳米颗粒ag-cunps溶液在检测hg2+方面的应用。一种检测hg2+的方法,将一种双金属银铜纳米颗粒ag-cunps溶液与待测样品等体积混合,紫外分光光度计读取吸光值。一种双金属银铜纳米颗粒ag-cunps溶液在催化降解硝基酚类化合物和铁氰化钾方面的应用;所述的硝基酚类化合物为邻硝基苯酚(2-np)、间硝基苯酚(3-np)、对硝基苯酚(4-np)和\或对硝基苯硫酚(4-ntp)。一种硝基酚类化合物和铁氰化钾的催化降解剂,它包括:一种双金属银铜纳米颗粒ag-cunps溶液和硼氢化钠溶液。本发明提供了一种双金属银铜纳米颗粒,是硫酸铜和柠檬酸钠通过水相氧化还原,利用硼氢化钠作为还原剂,合成双金属银铜纳米颗粒,利用其溶液通过反应前后紫外吸收峰值的变化同时伴随着颜色变化的特性来检测重金属汞离子,结果表明,双金属银铜纳米颗粒组成的比色探针对汞离子具有较好的灵敏度和选择性,并且具有较好的环境适应性,双金属银铜纳米颗粒还具有高效的催化效果,利用硼氢化钠催化降解硝基酚类化合物和铁氰化钾,本方法具有节约贵金属、成本低、合成方法简单、易操作、可视化和便于推广等特点。附图说明图1ag-cunps和相同浓度的不同金属离子混合的紫外吸收光谱图;b、ag-cunps和相同浓度的不同金属离子比色图像;图2a、ag-cunpstem;b、ag-cunps加入hg2+之后tem;c、ag-cunps粒子尺寸分布柱状图;d、ag-cunps加入hg2+之后粒子尺寸分布柱状图;图3a、ag-cunps加入不同浓度的hg2+的紫外吸收光谱图;b、ag-cunps加入不同浓度的hg2+的比色图片;图4ag-cunps加入含有各种金属离子的湖水样品后紫外吸收光谱图,所有金属离子浓度为50μm;b、ag-cunps与含有各种金属离子的湖水样品混合比色图;图5ag-cunps加入湖水配制的不同浓度hg2+紫外吸收光谱图;b、不同浓度的hg2+与a482/a406线性关系图;c、比色图片;图6在ag-cunps存在下硼氢化钠还原4-np的紫外吸收光谱图;b、ln[c(t)/c(0)]与反应时间线性关系图;图7在ag-cunps存在下硼氢化钠还原k3fe(cn)6紫外吸收光谱图;b、ln[a(t)/a(0)]与反应时间线性关系图。具体实施方式实施例1双金属银铜纳米颗粒(ag-cunps)溶液的制备向烧瓶内加入20ml超纯水,然后在磁力搅拌下加入50μl0.1m的硫酸铜和50μl0.1m的柠檬酸钠的混合溶液,并迅速加入新配制的1ml硼氢化钠(3.8mg加入4mlh2o)到搅拌溶液中。这时形成的溶液为铜纳米颗粒溶液,大约15min后,加入50μl0.1m的硝酸银溶液,继续磁力搅拌20min,溶液的颜色由浅黄色变成了黄色,即可得到双金属银铜纳米颗粒溶液。实施例2双金属银铜纳米颗粒(ag-cunps)的检测应用1、选择性测试双金属银铜纳米颗粒(ag-cunps)比色探针具有很强的光学性质及检测性能,并且此探针的制备简单,节约贵金属成本,所以合成的ag-cunps作为纳米比色探针。ag-cunps比色探针检测hg2+的过程中,待测的样品与ag-cunps溶液按体积比为1:1进行混合,即200µl的hg2+溶液样品加入到200µl的ag-cunps溶液中,所有的选择性实验和灵敏度实验都按以上的比例进行,具体实验过程如下:200µlag-cunps溶液中分别加入200µl的相同浓度(50μm)不同的重金属离子(fe2+,mn2+,cr3+,cu2+,ba2+,ca2+,cd2+,co2+,ni2+,pb2+,zn2+,mg2+和hg2+),通过肉眼观察,加入hg2+的混合溶液颜色由原来的黄色变为浅橙色。而其他混合溶液的颜色与空白试样溶液颜色相同为黄色,这可以清晰地区别出hg2+的样品。之后,将混合溶液加入到比色皿中放到紫外分光光度计中进行测试,通过紫外吸收光谱图可以看出加入hg2+的混合溶液吸收峰发生蓝移,在370nm处有特征吸收峰,并且在482nm处出现第二个吸收峰,而其他混合溶液的紫外吸收峰对比空白试样没有发生变化(如图1),此外,使用透射电子显微镜(tem)测试加入hg2+前后的混合溶液,可以观察到前后溶液颗粒大小发生变化(如图2a,2b)并通过计算可知制备的ag-cunps颗粒尺寸大约是9nm左右,加入50μm的hg2+后发现尺寸明显变大,大约是19nm左右(如图2c,2d)。从以上结果可知双金属银铜纳米颗粒能够检测出水溶液样品中含有的微量的重金属离子hg2+。2、灵敏度测试(1)200µlag-cunps中分别加入不同浓度200µl的hg2+溶液(0-50μm),从紫外光谱(图3a)中可以看出,向其中加入不同浓度的hg2+,发现随着hg2+浓度的升高,ag-cunps混合溶液的吸收强度逐渐降低,溶液颜色也发生了明显变化。当hg2+浓度为50μm时,ag-cunps的吸收强度降低最多,颜色也由原来的黄色变为浅橙色(如图3)。进行灵敏度的检测时,ag-cunps作为探针的吸收强度比值a482/a406与1-5nm浓度的hg2+有良好的线性关系。计算可知最低检测浓度为2.5nm。因此,ag-cunps可以作为检测hg2+的比色探针快速并定量地检测水溶液中hg2+的存在。(2)取自校园湖水的水样配制浓度为50μm不同的重金属离子使其与探针以体积比1:1进行混合用紫外光谱测试实际混合样品的特征吸收峰,测试实际样品的选择性(如图4)。从图中可知,此探针还是对hg2+有响应。之后,我们用湖水配制不同浓度的hg2+(0.001-50μm),使其与探针以体积比1:1进行混合测试实际样品的灵敏度(如图5)。从图中可知,混合溶液吸收强度比值a482/a406与1-5nm浓度的hg2+有良好的线性关系且该探针在实际水样中的最低检测浓度为0.25nm。实施例3双金属银铜纳米颗粒(ag-cunps)的催化应用1、硝基酚类化合物的催化硝基酚类化合物包括邻硝基苯酚(2-np)、间硝基苯酚(3-np)、对硝基苯酚(4-np)和对硝基苯硫酚(4-ntp)。催化还原反应如下:2-np的催化还原:将90ul的0.01m2-np溶液和新制备600μl的0.5m硼氢化钠溶液混合,将混合溶液加入到1.0-3.0ml超纯水的比色皿中,然后,将30µlag-cunps作为催化剂加入到上述混合溶液中,没有任何搅拌操作,通过紫外吸收光谱监测反应情况。2-np通过30μl的ag-cunps被100%催化还原转化为2-ap。该催化反应时间是490s,而且ln[a(t)/a(0)]和反应时间(t)呈线性关系,速率常数是k=5.96×10-3s-1,相关系数r2=0.9741。3-np的催化还原:将150ul的0.01m3-np溶液和新制备1.0ml的0.5m硼氢化钠溶液混合,将混合溶液加入到有1.0-3.0ml超纯水的比色皿中,然后,将30ulag-cunps作为催化剂加入到上述混合溶液中,没有任何搅拌操作,通过紫外吸收光谱监测反应情况。ag-cunps作为还原剂还原转化为3-ap。该催化反应在140s就已经完全反应且速率常数是k=18.8×10-3s-1,相关系数r2=0.9716。4-np的催化还原:将25ul的0.01m4-np溶液和新制备200μl的0.4-0.7m硼氢化钠溶液混合加入到1.0-3.0ml超纯水于比色皿中,然后,将30µlag-cunps作为催化剂加入到上述混合溶液,没有任何搅拌操作,通过紫外吸收光谱监测反应情况。结果见图6。在没有催化剂存在下,随着时间的推移,bh4-是无法还原相应的氨基化合物和减少4-np在400nm的峰值强度,这验证还原反应不会发生。然而,加入30μl的ag-cunps作为催化剂后,可以看出随着反应的进行在400nm处峰值逐渐降低,同时,氨基酚类逐渐生成,新的吸收峰在315nm逐渐形成并升高,反应时间是595s。通过ln[c(t)/c(0)]和反应时间的线形关系图可知反应的速率常数(k)是7.74×10-3·s-1。4-ntp的催化还原:将25ul的0.01m4-ntp溶液和新制备200μl的0.5m硼氢化钠溶液混合加入到1.0-3.0ml超纯水于比色皿中,然后,将30µlag-cunps作为催化剂加入到上述混合溶液,没有任何搅拌操作,通过紫外吸收光谱监测反应情况。2、k3fe(cn)6的催化还原将0.3-0.5ml8×10-3mk3fe(cn)6加入到20-40µlag-cunps催化剂,随后,快速加入适量冰冷的新制备的硼氢化钠溶液。利用紫外分光光度计快速测试上述混合溶液,通过紫外吸收光谱监测反应情况。结果见图7。k3[fe(cn)6]溶液的吸收波长在λ=420nm,加入新配制的硼氢化钠溶液后,随着k4[fe(cn)6]的形成,吸收强度逐渐降低。在给定的条件下,30μl的ag-cunps溶液催化还原k3(fe(cn)6)溶液在210s内(图7a),图7b所示,催化反应的速率常数(k)为18.2×10-3·s–1。然而该实验如果没有催化剂存在下要持续反应12h才可以结束。这个结果展示了ag-cunps的高效催化效果。表1银铜纳米颗粒作为催化剂催化还原硝基酚类化合物和铁氰化钾反应物和催化剂用量反应物反应物用量nabh4用量催化剂用量邻硝基苯酚(2-np)0.01m,90ul0.5m,600μl30ul间硝基苯酚(3-np)0.01m,150ul0.5m,1ml30ul对硝基苯酚(4-np)0.01m,25ul0.5m,200μl30ul对硝基苯硫酚(4-ntp)0.01m,25ul0.5m,200μl30ul铁氰化钾(k3fe(cn)6)8×10-3m,400ul0.04m,800μl30ul当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1