一种双核镁‑锗钨氧簇催化剂、制备方法及其用途与流程
本发明属于多金属氧簇催化剂材料制备技术领域,其中涉及到一种双核镁-锗钨氧簇催化剂的制备技术,为其催化应用奠定基础。
技术背景
多金属氧簇化学发展至今已经历了近两百多年的历史,已经成为当前无机化学中发展最快、交叉最广的领域之一。早期的多金属氧簇化学认为无机含氧酸(如磷酸、硫酸、钨酸、钼酸等)经缩合可形成缩合酸。多金属氧簇化学就是关于同多酸和杂多酸的化学,前者涉及同多阴离子,后者涉及杂多阴离子。在多金属氧簇中,钨能形成许多的同多及杂多钨氧簇合物。实验表明,该类化合物在催化、相转移、选择性氧化及药物化学方面具有较好的前景。
硫醚氧化为相应的砜类化合物是有机合成及工业生产的重要反应。究其原因是因为硫醚氧化物亚砜和砜具有良好的生物活性,在农药、医药等精细化学品中得到广泛的应用。重要的是,砜和亚砜是有机合成反应中重要的合成中间体,在合成功能材料和分子重组等反应中具有广阔的应用前景。其主要用作制造染料、医药、香料、调味品、农药等重要中间体的原料。在硫醚氧化反应中,H2O2作为绿色氧化剂而备受关注,可是H2O2作为氧化剂存在的问题是其氧化能力中等。因此,为了较好地以H2O2作为氧化剂实现绿色氧化硫醚化合物的主要问题是建立高效、高选择性的催化体系。因此选择合适的催化剂成为解决这一问题的关键。
近年来,文献报道中有机无机杂化的钨磷氧簇(Ezzat Rafie, et al, Journal of Molecular Catalysis A: Chemical, 2013,380, 18-27)氧化苯硫醚,但是在以上反应中存在着催化剂合成较为复杂等问题。
基于以上文献的基础上,设计一个硫醚氧化生成砜、合成简单的高效催化体系是十分必要的。通过检索,尚未发现与本发明申请相关的公开专利文献。
技术实现要素:
本项发明的目的是解决以往催化剂在双氧水为氧化剂下硫醚的选择性氧化过程中合成较为复杂等问题。提供了一种合成新型双核镁-锗钨氧簇催化剂的制备方法,以期在硫醚的选择性氧化中具有较好的催化作用,实现硫醚分子选择性氧化的目标。
本发明的方案是,双核镁-锗钨氧簇催化剂,其特征是,结构式为:
双核镁-锗钨氧簇催化剂的制备方法,将金属镁盐、DMF在水溶液中与锗钨酸反应构筑金属双核镁-锗钨氧簇;利用自然挥发法得到双核镁-锗钨氧簇催化剂的单晶。
所述的制备方法,优选的是,在一个洁净的烧杯中依次加入氯化镁、N,N’-二甲基甲酰胺(DMF)溶解在水中, 搅拌溶解,再加入锗钨酸,加热搅拌,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体,产率约47~62%。
所述的制备方法,优选的是,在30~50℃下搅拌6~10h(优选的,在40℃下搅拌8 h)。
所述的制备方法,优选的是,氯化镁:N,N’-二甲基甲酰胺:锗钨酸物质的量之比为2~4 : 15~30 : 1~3。
本发明还提供了所述锶-锗钨氧簇催化剂在硫醚选择性氧化中的用途。硫醚为苯甲硫醚、对氯苯甲硫醚、对硝基苯甲硫醚、对甲氧基苯甲硫醚等。
本发明的设计思路如下:
将金属镁盐与DMF在水溶液中与锗钨酸发生取代反应构筑双核镁-锗钨氧簇配合物;并利用自然挥发法得到了双核镁-锗钨氧簇催化剂的单晶;
将具有明确结构的双核镁-锗钨氧簇催化剂应用于硫醚的双氧水条件下选择性催化氧化中,实现硫醚选择性氧化的高转化率高选择性的目标。
这类催化剂的晶体结构信息通过如下方法获得的:
通过常规的溶液反应合成得到双核镁-锗钨氧簇催化剂的晶体,具体的描述实验方法如下:
在100mL的烧杯中依次加入氯化镁(2 ~4mmol)、DMF(15 ~30mmol)以及水 50 ~80 mL, 搅拌溶解,再加入锗钨酸(1 ~3mmol),在30~50 ℃下搅拌6~10h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约47~59%。
产品通过单晶X衍射,元素分析进行表征,得到关于晶体结构的准确信息。具体的结果如下:
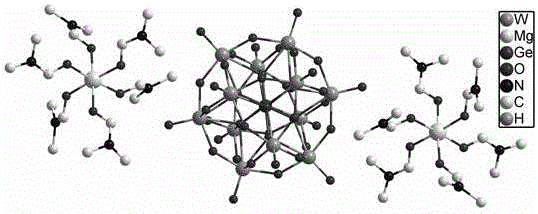
晶体的分子式为[Mg(HCON(CH3)6]2GeW12O40, 其中阳离子部分为金属镁与DMF形成的配合阳离子,阴离子为GeW12O40,二者通过静电引力相互作用结合在一起。
这项发明主要是合成双核镁-锗钨氧簇催化剂,已经将其应用于硫醚类化合物的选择性氧化。这类催化剂可以实现硫醚化合物的选择性氧化,转化率高达92.7%,选择性高达94.9%。该类催化剂的制备方法反应过程简单。
上述硫醚为苯甲硫醚、对氯苯甲硫醚、对甲基苯甲硫醚、对甲氧基苯甲硫醚等,转化率,选择性通过气相色谱检测。
本发明提供双核镁钨氧簇催化剂具有以下特点:
制备方法简单、并且催化剂都具有明确的分子结构,有利于研究催化反应机理。
催化剂便于容易分离,经处理后可以多次使用,并且仍能保持良好的催化活性,有利于工业化生产。
附图说明
图1. 化合物[Mg(HCON(CH3)6]2GeW12O40的晶体结构。
具体实施方式
下面结合实施例对本发明作详细描述,但保护范围不被此限制。
本发明所用原料皆可从市场购买,比如DMF全称N,N’-二甲基甲酰胺,购自国药集团化学试剂有限公司。
实施例1:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(2mmol)、DMF(16mmol)以及水50mL, 搅拌溶解,再加入锗钨酸(1mmol),在40℃下搅拌6h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约56%。
实施例2:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(3mmol)、DMF(30mmol)以及水50 mL, 搅拌溶解,再加入锗钨酸(2mmol),在50℃下搅拌10h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约52%。
实施例3:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(4mmol)、DMF(15mmol)以及水80 mL, 搅拌溶解,再加入锗钨酸(3mmol),在30℃下搅拌6h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约49%。
实施例4:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(4mmol)、DMF(30mmol)以及水50mL, 搅拌溶解,再加入锗钨酸(1mmol),在30℃下搅拌8h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约47%。
实施例5:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(3mmol)、DMF(20mmol)以及水70 mL, 搅拌溶解,再加入锗钨酸(2mmol),在50 ℃下搅拌10h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约61%。
实施例6:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(4mmol)、DMF(30mmol)以及水50mL, 搅拌溶解,再加入锗钨酸(2mmol),在40 ℃下搅拌8h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约55%。
实施例7:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(2mmol)、DMF(15mmol)以及水60mL, 搅拌溶解,再加入锗钨酸(3mmol),在30℃下搅拌6h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约51%。
实施例8:化合物[[Mg(HCON(CH3)6]2GeW12O40的制备
在100mL的烧杯中依次加入氯化镁(2mmol)、DMF(30mmol)以及水70 mL, 搅拌溶解,再加入锗钨酸(2mmol),在40℃下搅拌8h,冷却至室温,过滤,滤液在室温下缓慢蒸发,4~6天后得到无色晶体[Mg(HCON(CH3)6]2GeW12O40。产率约58%。
实施例9:化合物[[Mg(HCON(CH3)6]2GeW12O40多金属氧簇催化剂对硫醚类化合物的催化氧化应用
以化合物[[Mg(HCON(CH3)6]2GeW12O40为例:取0.25mmol硫醚溶于1 mL甲醇中,0.3mmol双氧水,加入催化剂20mg, 40 °C下反应4-8小时,用气相色谱检测,具体硫醚氧化的数据见表2.
表2. 化合物[Mg(HCON(CH3)6]2GeW12O40 对硫醚选择性氧化结果列表
图1为化合物[[Mg(HCON(CH3)6]2GeW12O40的晶体结构。
表1为该化合物的晶体学数据。
表1
- 还没有人留言评论。精彩留言会获得点赞!
- 一种高性能抗指纹剂的制备方法
- 一种常压下光催化合成苯胺类化合物的方法及其使用的催化剂的利记博彩app
- 一种底物按次序催化的金属纳米粒子基催化剂的利记博彩app
- 一种Cu?ZnO?ZrO<sub>2</sub>?NH<sub>2</sub>/SBA?15复合催化剂的制备方法及其应用
- 一种催化气化灰渣中不可溶性碱金属催化剂的回收方法
- 一种催化氧化丙烷制取丙烯酸的催化剂及其制备方法
- 催化氧化丙烷制取丙烯酸的催化剂及其制备方法
- 一种催化合成γ-氯丙基三氯硅烷的方法及其催化剂的利记博彩app
- 一种高性能氧还原MnO<sub>2</sub>-Mn<sub>3</sub>O<sub>4</sub>/碳纳米管复合催化剂及其制备方法和应用
- 锡类催化剂催化合成聚乳酸共聚改性产物的方法