一种红色发光材料及其制备方法与流程
本发明涉及发光材料技术领域,尤其是涉及一种红色发光材料及其制备方法。
背景技术:
新型光源白光led由于具有体积小、能耗低、寿命长、无污染等诸多优点而具有重要的应用价值和广阔的市场前景。目前,白光led备受世界各国的大力推广,有望取代传统的照明光源如荧光灯和白炽灯,成为新一代绿色照明光源。
然而,当前白光led的制造还面临着一大问题:由于蓝光芯片+黄色荧光粉(yag:ce3+)合成的白光中缺少红光成分从而导致高色温、低显色指数的冷白光。这直接造成此类白光led在照明上,人眼感觉光线阴冷,显色性差。为了满足室内照明的需求,需要加入合适比例的红色荧光粉来改善led的色温和显色指数。目前市场上已经有一些eu2+掺杂的氮化物高效红色荧光粉和mn4+掺杂的氟化物红色荧光粉等。但是,氮化物红色荧光粉制备条件苛刻,需要高温高压,成本较高;氟化物红色荧光粉制备工艺复杂且制备过程所要用到的试剂对环境污染较大。
因此,有必要开发一种制备简单、廉价且环保的红色荧光粉,以实现高显色指数,低色温白光led照明。利用mn(iv)离子作为发光中心,避免了稀土离子的使用,可以降低成本。将其掺杂到合适的金属氧化物中可实现较好的红光发射。但现有技术公开报道的相关研究其制备温度都较高,一般大于1000℃,并且制备工艺复杂。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种红色发光材料,本发明提供的发光材料由蓝光led芯片激发产生红色发射光谱,并且本发明的红色荧光粉制备工艺简单,合成温度低。
本发明提供了一种红色发光材料,为式(ⅰ)所示结构:
li2mg3a1-xo6-yf2y:xmn4+;式(ⅰ);
其中,a选自ti4+、zr4+或hf4+中的一种或多种;x为掺杂的mn4+离子的摩尔数;0<x≤0.04;0<y<1.5。
优选的,所述0.01<x≤0.04;0.1<y<1.5。
本发明提供了一种如上述技术方案所述的红色发光材料的制备方法,包括如下步骤:
a)将含锂化合物、含镁化合物、含a化合物、含氟化合物以及含锰化合物按照比例混合,研磨,得到混合物;所述含a化合物选自含钛化合物、含锆化合物和含铪化合物中的一种或几种;所述含锂化合物、含镁化合物、含a化合物、含氟化合物和含锰化合物的混合摩尔比为2:3:(1-x):2y:x;
b)将所述混合物加热煅烧、研磨,得到红色发光材料;所述煅烧温度为900℃~980℃。
优选的,步骤b)所述煅烧在空气的环境下进行。
优选的,步骤b)所述煅烧的温度为920℃~960℃;煅烧的时间为2~6h。
优选的,步骤b)所述煅烧后为冷却,所述冷却为自然冷却;所述冷却后的温度为20~30℃。
优选的,步骤a)所述含锂化合物为含锂元素的碳酸盐或含锂的硝酸盐;所述含镁化合物为含镁元素的碳酸盐、含镁元素的硝酸盐、含镁元素的草酸盐或含镁元素的氧化物;所述含钛化合物为含钛元素的氧化物;所述锆化合物为含锆元素的氧化物;所述铪化合物为含铪元素的氧化物;所述含氟化合物为含氟元素的碱金属氟化物;所述含锰化合物为含锰元素的碳酸盐、含锰元素的草酸盐、含锰元素的氧化物或含锰元素的硝酸盐。
优选的,步骤a)所述含锂化合物为碳酸锂或硝酸锂;所述含镁化合物为碱式碳酸镁或氧化镁;所述含钛化合物为氧化钛;所述含锆化合物为氧化锆;所述含铪化合物为氧化铪;所述含氟化合物为氟化锂;所述含锰化合物为碳酸锰或氧化锰。
优选的,步骤a)所述研磨为手动研磨,所述研磨时间为30~90min。
优选的,步骤b)所述研磨为手动研磨,所述研磨时间为30~90min。
与现有技术相比,本发明提供了一种红色发光材料,为式(ⅰ)所示结构:li2mg3a1-xo6-yf2y:xmn4+;式(ⅰ);其中,a选自ti4+、zr4+或hf4+中的一种或多种;x为掺杂的mn4+离子的摩尔数;0<x≤0.04;0<y<1.5。本发明提供的红色发光材料可由蓝光led芯片激发产生红色发射光谱;并且本发明采用的红色发光材料以mn(iv)离子作为发光中心,避开了传统发光材料经常使用的稀土离子,大降低了原料采购的成本,减少了稀土资源的消耗。另一方面,该材料的反应温度低于1000℃,相比于市场上其他的红色荧光粉,反应温度在很大程度上得到降低,大大降低了电能消耗,节约了生产成本。
附图说明
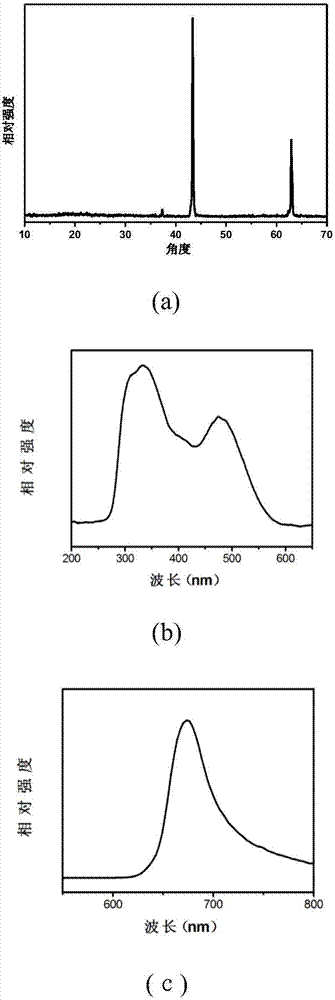
图1(a)为本发明实施例2所制备的红色荧光粉的xrd图谱;图1(b)和(c)分别为本发明实施例2所制备的红色荧光粉激发和发射光谱;
图2(a)和(b)分别为本发明实施例3所制备的红色荧光粉激发和发射光谱;
图3(a)和(b)分别为本发明实施例6所制备的红色荧光粉激发和发射光谱;
图4(a)和(b)分别为本发明实施例11所制备的红色荧光粉激发和发射光谱;
图5(a)和(b)分别为本发明实施例13所制备的红色荧光粉激发和发射光谱;
图6(a)和(b)分别为本发明实施例17所制备的红色荧光粉激发和发射光谱;
图7(a)和(b)分别为本发明实施例18所制备的红色荧光粉激发和发射光谱;
图8(a)和(b)分别为本发明实施例19所制备的红色荧光粉激发和发射光谱。
具体实施方式
本发明提供了一种红色发光材料,为式(ⅰ)所示结构:
li2mg3a1-xo6-yf2y:xmn4+;式(ⅰ);
其中,a选自ti4+、zr4+或hf4+中的一种或多种;x为掺杂的mn4+离子的摩尔数;0<x≤0.04;优选的,所述0.01<x≤0.04;更优选的,所述0.02<x≤0.03;
其中,2y为氟元素的摩尔数,0<y<1.5,优选的,0.1<y<1.5;更优选的,0.3<y<1.3;最优选的,0.5<y<1.2。
本发明提供了一种红色发光材料,为式(ⅰ)所示结构:li2mg3a1-xo6-yf2y:xmn4+;式(ⅰ);其中,a选自ti4+、zr4+或hf4+中的一种或多种;x为掺杂的mn4+离子的摩尔数;0<x≤0.04;0<y<1.5。本发明提供的红色发光材料可由蓝光led芯片激发产生红色发射光谱;并且本发明采用的红色发光材料以mn(iv)离子作为发光中心,避开了传统发光材料经常使用的稀土离子,大降低了原料采购的成本,减少了稀土资源的消耗。另一方面,该材料的反应温度低于1000℃,相比于市场上其他的红色荧光粉,反应温度在很大程度上得到降低,大大降低了电能消耗,节约了生产成本。
本发明其中一部分实施例中,红色发光材料的化学组成为li2mg3ti0.995o5.842f0.316:0.005mn4+。;
本发明其中一部分实施例中,红色发光材料的化学组成为li2mg3ti0.995o5.682f0.636:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为li2mg3ti0.995o5.206f1.588:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为li2mg3ti0.995o5.576f0.848:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为li2mg3ti0.995o5.472f1.056:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.995o5.366f1.268:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.9999o5.367f1.267:0.0001mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.9995o5.367f1.267:0.0005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.999o5.366f1.268:0.001mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.997o5.366f1.268:0.003mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.995o5.366f1.268:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.99o5.364f1.272:0.01mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.985o5.362f1.276:0.015mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.98o5.362f1.276:0.02mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.97o5.358f1.284:0.03mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3ti0.96o5.356f1.288:0.04mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3sn0.995o5.204f1.592:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3zr0.995o5.266f1.469:0.005mn4+;
本发明其中一部分实施例中,红色发光材料的化学组成为化学组成为li2mg3hf0.995o5.063f1.873:0.005mn4+。
本发明提供了一种如上述技术方案所述的红色发光材料的制备方法,包括如下步骤:
a)将含锂化合物、含镁化合物、含a化合物、含氟化合物以及含锰化合物按照比例混合,研磨,得到混合物;所述含a化合物选自含钛化合物、含锆化合物和含铪化合物中的一种或几种;所述含锂化合物、含镁化合物、含a化合物、含氟化合物和含锰化合物的混合摩尔比为2:3:(1-x):2y:x;
b)将所述混合物加热煅烧、研磨,得到红色发光材料;所述煅烧温度为900℃~980℃。
本发明提供的红色发光材料的制备方法首先将含锂化合物、含镁化合物、含a化合物、含氟化合物以及含锰化合物按照比例混合,研磨,得到混合物。
本发明对于所述混合比例不进行限定,本领域技术人员熟知的即可。
按照本发明,所述含锂化合物、含镁化合物、含a化合物、含氟化合物和含锰化合物的混合摩尔比优选为2:3:(1-x):2y:x;其中,0<x≤0.04;优选的,所述0.01<x≤0.04;更优选的,所述0.02<x≤0.03;0<y<1.5,优选的,0.1<y<1.5;更优选的,0.3<y<1.3;最优选的,0.5<y<1.2。
本发明对于所述研磨的方式不进行限定,本领域技术人员熟知的即可;优选为手动研磨;所述研磨的时间优选为30~90min;更优选为30~60min。笨本发明优选在玛瑙研钵中进行研磨。
按照本发明,所述含锂化合物优选为含锂元素的碳酸盐或含锂的硝酸盐;更优选为碳酸锂或硝酸锂;
所述含镁化合物优选为含镁元素的碳酸盐、含镁元素的硝酸盐、含镁元素的草酸盐或含镁元素的氧化物;更优选为碱式碳酸镁或氧化镁。
所述含钛化合物优选为含钛元素的氧化物;更优选为氧化钛。
所述含锆化合物优选为含锆元素的氧化物;更优选为氧化锆。
所述铪化合物为含铪元素的氧化物;更优选为氧化铪。
所述含氟化合物为含氟元素的碱金属氟化物;更优选为氟化锂。
所述含锰化合物为含锰元素的碳酸盐、含锰元素的草酸盐、含锰元素的氧化物或含锰元素的硝酸盐;更优选为碳酸锰或氧化锰。
得到混合物后,将所述混合物加热煅烧、研磨,得到红色发光材料。
本发明对于所述煅烧的方式不进行限定,本领域技术人员熟知的即可,优选将混合物放置于刚玉坩埚中,在马弗炉中煅烧。
按照本发明,所述煅烧在空气的环境下进行。所述煅烧温度为900℃~980℃;优选为920℃~960℃;所述煅烧的时间优选为2~6h;更优选为3~6h;最优选为4~6h。
按照本发明,所述煅烧后为冷却,所述冷却为自然冷却;所述冷却后的温度优选为20~30℃。
冷却后研磨,得到红色发光材料。
本发明对于所述研磨的方式不进行限定,本领域技术人员熟知的即可;优选为手动研磨;所述研磨的时间优选为30~90min;更优选为30~60min。笨本发明优选在玛瑙研钵中进行研磨。
本发明制备条件要求较低,工艺流程简单易行,可重复性较好,所需要原材料廉价且丰富。该材料能被蓝光led芯片激发并发出红光。该类材料采用mn(iv)离子作为发光中心,避开了传统发光材料经常使用的稀土离子,大降低了原料采购的成本,减少了稀土资源的消耗。另一方面,该材料的反应温度低于1000℃,相比于市场上其他的红色荧光粉,反应温度在很大程度上得到降低,大大降低了电能消耗,节约了生产成本。
为了进一步说明本发明,以下结合实施例对本发明提供的红色发光材料及其制备方法进行详细描述。
实施例1
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.082g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.995o5.842f0.316:0.005mn4+。
实施例2
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.165g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图1(a)为本发明实施例2所制备的红色荧光粉的xrd图谱;图1(b)和(c)分别为本发明实施例2所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3ti0.995o5.682f0.636:0.005mn4+。
实施例3
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.412g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图2(a)和(b)分别为本发明实施例3所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3ti0.995o5.206f1.588:0.005mn4+。
实施例4
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.220g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.995o5.576f0.848:0.005mn4+。
实施例5
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.274g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.995o5.472f1.056:0.005mn4+。
实施例6
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.329g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图3(a)和(b)分别为本发明实施例6所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3ti0.995o5.366f1.268:0.005mn4+。
实施例7
准确称量出原材料:1.108g碳酸锂、1.80g氧化镁、1.198g二氧化钛、0.0002g碳酸锰以及0.493g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.9999o5.367f1.267:0.0001mn4+。
实施例8
准确称量出原材料:1.108g碳酸锂、1.80g氧化镁、1.198g二氧化钛、0.0009g碳酸锰以及0.493g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.9995o5.367f1.267:0.0005mn4+。
实施例9
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.001g碳酸锰以及0.329g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.999o5.366f1.268:0.001mn4+。
实施例10
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.003g碳酸锰以及0.329g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.997o5.366f1.268:0.003mn4+。
实施例11
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.006g碳酸锰以及0.329g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图4(a)和(b)分别为本发明实施例11所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3ti0.995o5.366f1.268:0.005mn4+。
实施例12
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.011g碳酸锰以及0.330g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.99o5.364f1.272:0.01mn4+。
实施例13
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.017g碳酸锰以及0.331g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图5(a)和(b)分别为本发明实施例13所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3ti0.985o5.362f1.276:0.015mn4+。
实施例14
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.023g碳酸锰以及0.331g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至980℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.98o5.362f1.276:0.02mn4+。
实施例15
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.034g碳酸锰以及0.333g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧8小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.97o5.358f1.284:0.03mn4+。
实施例16
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、0.799g二氧化钛、0.046g碳酸锰以及0.334g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至930℃煅烧10小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。化学组成为li2mg3ti0.96o5.356f1.288:0.04mn4+。
实施例17
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、1.50g二氧化锡、0.006g碳酸锰以及0.413g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图6(a)和(b)分别为本发明实施例17所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3sn0.995o5.204f1.592:0.005mn4+。
实施例18
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、1.23g二氧化锆、0.006g碳酸锰以及0.381g的氟化锂。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图7(a)和(b)分别为本发明实施例18所制备的红色荧光粉激发和发射光谱。化学组成为li2mg3zr0.995o5.266f1.469:0.005mn4+。
实施例19
准确称量出原材料:0.739g碳酸锂、1.20g氧化镁、2.105g二氧化铪、0.006g碳酸锰以及0.486g的氟化锂。。将这些原材料在玛瑙研钵中研磨混合均匀后,再将所得混合物置于刚玉坩埚中。然后将其放入马弗炉内在空气环境下升温至950℃煅烧6小时。最后,待其自然冷却至室温后,取出再次研磨得到的粉红色粉末为最终产品。图8(a)和(b)分别为本发明实施例19所制备的红色荧光粉激发和发射光谱。li2mg3hf0.995o5.063f1.873:0.005mn4+。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!