一种赖氨酸分枝二聚多肽及其应用的利记博彩app
(一)技术领域
本发明涉及一种赖氨酸分枝二聚多肽及其应用。
(二)
背景技术:
自20世纪90年代从酵母蛋白中发现了自组装多肽以来,自组装多肽领域的研究得到了快速的发展,并已成功应用于生物技术、纳米材料、细胞工程、药物控释等领域(uspatentno.5670483,1997;no.5955343,1999;no.20020160471,2002;no.6548630,2003)。从天然蛋白衍生的自组装多肽都是利用l型氨基酸进行分子自组装,具有较好的生物相容性,能够被l型生物酶降解。
公开号为cn101054409a的中国专利申请公开了一种两亲型短肽,此短肽命名为d-eak,是用d型氨基酸构建的自组装短肽。d型氨基酸的自组装短肽,它一般不能被常规l型酶降解,体内稳定存在的时间相对较长。实验表明,d-eak短肽可在制备温控型、酸碱性分子器件或者生物分子探针中应用,可在制备保湿锁水剂中应用,可在细胞培养中应用,可在制备抑菌药物中应用。实验还表明,d-eak短肽形成的纳米纤维较短,使其的应用范围受到一定的限制。
公开号为cn101337985a的中国专利申请公开了另一种两亲型d自组装多肽,命名为d-rad16。实验表明,d-rad16自组装多肽形成的水凝胶可在制备保湿锁水剂中应用并对创伤有快速止血功能,可以通过添加药学上可接受的载体或者赋形剂制备成适合于临床使用的止血药物。d-rad16自组装多肽形成的纳米纤维支架支持多种细胞的生长,可作为细胞的三维培养基质材料,为新药研发提供一种可模拟体内环境的药物筛选模式。但是d型氨基酸的自组装短肽一般不能被常规l型酶降解,生物相容性较差,临床应用风险大。
(三)
技术实现要素:
本发明目的是提供一种新型的两亲型自组装多肽。通过赖氨酸分枝形成的二聚多肽,其分子间通过非共价键相互作用自发组合,由此而形成的自组装结构有更多的结构灵活性和多样性,促进自组装多肽在纳米生物医学中的应用。
本发明采用的技术方案是:
本发明提供一种式(1)所示赖氨酸分枝二聚多肽:
式(1)中,peptide1(多肽1)和peptide2(多肽2)均为8-20个氨基酸组成的多肽。peptide1通过氨基酸序列c-端的羧基与赖氨酸ε-氨基形成酰胺键,peptide2通过氨基酸序列c-端的羧基与赖氨酸α-氨基形成酰胺键。所述peptide1,peptide2的n-端可以连接任何一种天然氨基酸,小分子修饰或者乙酰化封端。
进一步,所述peptide1和peptide2各自独立为下列之一:(1)(aa+aanaa-aan)n;(2)(aa-aanaa+aan)n;(3)(aanaa+aanaa-)n;(4)(aanaa-aanaa+)n,其中,aa+为精氨酸或赖氨酸;aa-为天门冬氨酸或谷氨酸;aan丙氨酸、异亮氨酸、亮氨酸、苯丙氨酸或缬氨酸,n为2-5之间的任意正整数。
进一步,所述peptide1和peptide2的氨基酸序列相同。
进一步,所述赖氨酸分枝二聚多肽为下列之一:
(1)
氨基酸序列为:(acradaradarada)2k-nh2;
(2)
氨基酸序列为:(acakaeakaeakaea)2k-nh2;
(3)
氨基酸序列为:(aceikieikieiki)2k-nh2;
(4)
氨基酸序列为:aceikieikieiki-k(acradaradarada)-nh2;
其中ac为乙酰化封端。
本发明所述赖氨酸分枝形成的二聚多肽按如下方法制备:采用fmoc氨基树脂和氨基酸以逐步偶联的fmoc固相多肽合成法(fmocspps)进行合成:从fmoc氨基树脂首先连接fmoc-lys(fmoc)-oh或者fmoc-lys(dde)-oh,然后去除保护基和相应的氨基酸逐步偶联进行合成。经过切割反应及反相制备色谱纯化,冻干得到赖氨酸分枝二聚多肽。
通过赖氨酸分枝形成的二聚多肽作为自组装多肽,其原理是分子间通过非共价键相互作用自发组合形成一种结构灵活、构造稳定、具有某些理化性能的分子聚集体或超分子纳米结构。由于多肽1、多肽2与赖氨酸通过共价单键相连,多肽1和多肽2可以形成直键状的二聚多肽或者任意角度的三维立体结构。由此而形成的自组装结构有更多的结构灵活性和多样性。
本发明还提供一种所述赖氨酸分枝二聚多肽在制备纳米纤维水凝胶中的应用。本发明通过赖氨酸分枝二聚多肽作为自组装多肽,在盐离子、细胞培养基等生理环境下能自组装形成纳米纤维水凝胶,可在制备纳米阻隔材料中应用。
本发明提供一种所述赖氨酸分枝二聚多肽在制备锁水保湿剂中的应用。本分明所述的赖氨酸分枝二聚多肽能形成非常优良的水凝胶,肽与水的质量比可以低于1:99,因此这种赖氨酸分枝二聚肽是一种高效的锁水性物质,可在制备锁水保湿剂中应用。
本发明提供一种所述赖氨酸分枝二聚多肽在制备止血药物中的应用。本发明所述的赖氨酸分枝二聚多肽对创伤有快速止血功能,可制备成适合于临床使用的快速止血药物。
本发明中一些常用的缩写及术语具有以下含义:
fmoc:芴甲氧羰基
tbu:叔丁基
hobt:1-羟基苯并三氮唑
dic:n,n'-二异丙基碳二亚胺
tfa:三氟醋酸
meoh:甲醇
spps:固相多肽合成法
本发明室温是指20-30℃。
与现有技术相比,本发明的有益效果主要体现在:目前文献报道的自组装多肽均为单一直链的多肽分子。本发明提供了一种新型的两亲型自组装多肽,通过赖氨酸分枝形成的二聚多肽,其分子间通过非共价键相互作用自发组合,由此而形成的自组装结构有更多的结构灵活性和多样性,促进自组装多肽在纳米生物医学中的应用。本发明赖氨酸分枝二聚多肽在盐离子、细胞培养基等生理环境下能自组装形成纳米纤维水凝胶,可在制备纳米阻隔材料中应用,是一种高效的锁水性物质,可在制备锁水保湿剂中应用;对创伤有快速止血功能,可制备成适合于临床使用的快速止血药物。
(四)附图说明
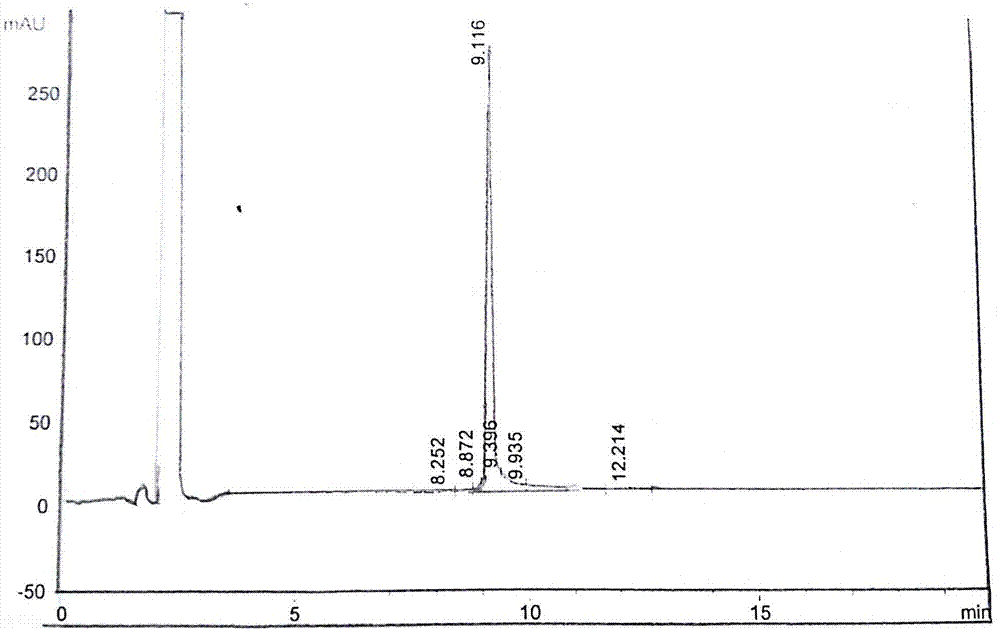
图1:实施例1制备的赖氨酸分枝二聚多肽的高效液相色谱(hplc)检测。
图2:实施例1制备的赖氨酸分枝二聚多肽的质谱检测。
图3:肝脏创伤出血模型(氯化钠注射液参照)。
图4:肝脏创伤出血模型(1%赖氨酸分枝二聚多肽(实施例1制备)溶液供试品)。
图5:股四头肌出血模型(氯化钠注射液参照)。
图6:股四头肌出血模型(1%赖氨酸分枝二聚多肽(实施例1制备)溶液供试品)。
(五)具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
实施例1赖氨酸分枝二聚多肽1的制备
1、材料
fmoc-rinkamidembharesin(笏甲氧羰基-rink酰胺树脂,购自chem-impexinternational,inc.catalog#06752)
fmoc-lys(fmoc)-oh(笏甲氧羰基-ε-笏甲氧羰基-赖氨酸)
fmoc-ala-oh(笏甲氧羰基-丙氨酸)
fmoc-asp(otbu)-oh(笏甲氧羰基-o-叔丁基-天冬氨酸)
fmoc-arg(pbf)-oh(笏甲氧羰基-γ-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基-精氨酸)
hobt(1-羟基苯并三氮唑)
dic(n,n-二异丙基碳二亚胺)
2、具体合成步骤:
所述多肽的合成采用从fmoc氨基树脂和氨基酸以逐步偶联的固相多肽合成法进行,工艺步骤如下:
步骤1.fmoc-rinkamidembha树脂(8mmol,20g,取代度0.4mmol/g)置于一多肽合成反应器中,用n,n-二甲基甲酰胺(300ml)溶胀30分钟。悬浮液过滤,去除滤液,将体积浓度20%哌啶/n,n-二甲基甲酰胺(300ml)加入到树脂中并搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,准备用于步骤2偶联。
步骤2.将11.2gfmoc-lys(fmoc)-oh(笏甲氧羰基-ε-笏甲氧羰基-赖氨酸),3.67g1-羟基苯并三氮唑(hobt)和3.79mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤1含有肽树脂的多肽合成反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将反应液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,去除洗涤液,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤3偶联。
步骤3.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤2含有肽树脂的多肽合成反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将反应液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤4偶联。
步骤4.将19.7gfmoc-asp(otbu)-oh(笏甲氧羰基-o-叔丁基-天冬氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤3含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将反应液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤5偶联。
步骤5.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤4含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将反应液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤6偶联。
步骤6.将31.1gfmoc-arg(pbf)-oh(笏甲氧羰基-γ-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基-精氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤5含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将反应液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤7偶联。
步骤7.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤6含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤8偶联。
步骤8.将19.7gfmoc-asp(otbu)-oh(笏甲氧羰基-o-叔丁基-天冬氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤7含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤9偶联。
步骤9.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤8含有的肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤10偶联。
步骤10.将31.1gfmoc-arg(pbf)-oh(笏甲氧羰基-γ-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基-精氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤9含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤11偶联。
步骤11.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤10含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤12偶联。
步骤12.将19.7gfmoc-asp(otbu)-oh(笏甲氧羰基-o-叔丁基-天冬氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤11含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤13偶联。
步骤13.将14.9gfmoc-ala-oh(笏甲氧羰基-丙氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤12含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤14偶联。
步骤14.将31.1gfmoc-arg(pbf)-oh(笏甲氧羰基-γ-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基-精氨酸),7.35g1-羟基苯并三氮唑(hobt)和7.57mln,n-二异丙基碳二亚胺(dic)溶于200ml的n,n-二甲基甲酰胺中,使氨基酸在0-10摄氏度活化20分钟。活化后,将溶液加入到步骤13含有肽树脂的反应器中,室温下偶联反应1-4个小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤肽树脂。然后肽树脂在体积浓度20%哌啶/n,n-二甲基甲酰胺溶液中搅拌30分钟以除去fmoc保护基。fmoc去保护后,将树脂用n,n-二甲基甲酰胺彻底洗涤,将洗涤后的肽树脂置于多肽合成反应器中,并准备用于步骤15偶联。
步骤15.将体积浓度10%醋酸酐/5%n-甲基吗啉/85%n,n-二甲基甲酰胺溶液(300ml)加入到步骤14含有肽树脂的反应器中进行多肽乙酰化封端,室温下偶联反应0.5-1小时,或直至茚三酮检测结果为阴性。将树脂悬浮液过滤并用n,n-二甲基甲酰胺洗涤五次,甲醇洗涤两次。室温真空下干燥后,得到肽树脂。
将所得的肽树脂悬浮在三氟醋酸切割液中,在室温(25℃)下搅绊反应2-5小时。过滤后,收集滤液并在乙醚中沉淀。将粗肽离心收集,用乙醚洗涤,并在室温真空下干燥,得到多肽粗品。经高效制备液相色谱纯化,冷冻干燥即得式(1)所示的赖氨酸分枝二聚多肽(acradaradarada)2k-nh2)。高效液相色谱(hplc)检测,结果见图1,根据图1中的谱峰面积确定其纯度达到了95%。质谱检测结果见图2,根据检测结果可确定其分子量为2709.8。
高效液相色谱(hplc)检测:美国安捷伦公司agilent1200型高效液相色谱仪。采用水和乙腈混合溶剂作流动相,c18分析色谱柱进行反相色谱检测。
质谱检测:美国热电公司tsq型质谱仪,esi电喷雾电离离子源。
实施例2赖氨酸分枝二聚多肽2
实施例2多肽的合成采用和实施例1相同的固相多肽合成法方法,从fmoc氨基树脂首先连接fmoc-lys(fmoc)-oh,然后去除fmoc保护基和相应的氨基酸逐步偶联进行合成,经过相同的切割反应及反相制备色谱纯化,冻干得到赖氨酸分枝二聚多肽2。所采用的树脂、氨基酸原料、偶联试剂如下:
fmoc-rinkamidembharesin(笏甲氧羰基-rink酰胺树脂,购自chem-impexinternational,inc.catalog#06752)
fmoc-lys(fmoc)-oh(笏甲氧羰基-ε-笏甲氧羰基-赖氨酸)
fmoc-lys(boc)-oh(笏甲氧羰基-ε-叔丁氧羰基-赖氨酸)
fmoc-ala-oh(笏甲氧羰基-丙氨酸)
fmoc-glu(otbu)-oh(笏甲氧羰基-o-叔丁基-谷氨酸)
hobt(1-羟基苯并三氮唑)
dic(n,n-二异丙基碳二亚胺)。
实施例3赖氨酸分枝二聚多肽3
实施例3多肽的合成采用和实施例1相同的固相多肽合成方法,从fmoc氨基树脂首先连接fmoc-lys(fmoc)-oh,然后去除fmoc保护基和相应的氨基酸逐步偶联进行合成,经过相同的切割反应及反相制备色谱纯化,冻干得到赖氨酸分枝二聚多肽3。所采用的树脂、氨基酸原料、偶联试剂如下:
fmoc-rinkamidembharesin(笏甲氧羰基-rink酰胺树脂,购自chem-impexinternational,inc.catalog#06752)
fmoc-lys(fmoc)-oh(笏甲氧羰基-ε-笏甲氧羰基-赖氨酸)
fmoc-lys(boc)-oh(笏甲氧羰基-ε-叔丁氧羰基-赖氨酸)
fmoc-ile-oh(笏甲氧羰基-异亮氨酸)
fmoc-glu(otbu)-oh(笏甲氧羰基-o-叔丁基-谷氨酸)
hobt(1-羟基苯并三氮唑)
dic(n,n-二异丙基碳二亚胺)。
实施例4赖氨酸分枝二聚多肽4
实施例4多肽的合成采用和实施例1相同的固相多肽合成方法,从fmoc氨基树脂首先连接fmoc-lys(dde)-oh,然后去除fmoc保护基和相应的氨基酸的逐步偶联进行合成。在树脂上首先完成aceikieikieiki的连接后,用2%水合并肼的dmf溶液搅拌脱去赖氨酸侧链氨基上的dde保护基,然后再逐个偶联相应的氨基酸完成acradaradarada的连接。经过相同的切割反应及反相制备色谱纯化,冻干得到赖氨酸分枝二聚多肽4。所采用的树脂、氨基酸原料、偶联试剂如下:
fmoc-rinkamidembharesin(笏甲氧羰基-rink酰胺树脂,购自chem-impexinternational,inc.catalog#06752
fmoc-lys(dde)-oh(笏甲氧羰基-ε-dde-赖氨酸)
fmoc-lys(boc)-oh(笏甲氧羰基-ε-叔丁氧羰基-赖氨酸)
fmoc-ala-oh(笏甲氧羰基-丙氨酸)
fmoc-ile-oh(笏甲氧羰基-异亮氨酸)
fmoc-asp(otbu)-oh(笏甲氧羰基-o-叔丁基-天冬氨酸)
fmoc-glu(otbu)-oh(笏甲氧羰基-o-叔丁基-谷氨酸)
fmoc-arg(pbf)-oh(笏甲氧羰基-γ-2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基-精氨酸)
hobt(1-羟基苯并三氮唑)
dic(n,n-二异丙基碳二亚胺)。
实施例5赖氨酸分枝二聚肽不同条件下形成水凝胶及其锁水性能
1、在不同盐作用下形成水凝胶
(1)将实施例1所得赖氨酸分枝二聚肽1用18.2mω·cm的纯净水制备成质量浓度为1%的赖氨酸分枝二聚多肽溶液。
(2)称取氯化钠或氯化钾或磷酸钠加入到纯净水中配制成0.15mol/l盐溶液,盐溶液的浓度范围在0.01-1mol/l皆可。
(3)加入等体积的盐溶液到赖氨酸分枝二聚多肽溶液中,自组装时间24小时。同样条件下,将实施例2-4制备的赖氨酸分枝二聚肽替换赖氨酸分枝二聚肽1进行实验,结果表明,实施例1-4制备的赖氨酸分枝二聚肽均能形成水凝胶,在肉眼下为透明胶体。
2、赖氨酸分枝二聚肽在细胞生长的生理环境下形成水凝胶
(1)取含10%胎牛血清的dmem培养基滴入96孔板,每孔100μl。
(2)将实施例1所得赖氨酸分枝二聚肽1用18.2mω·cm的纯净水制备成质量浓度为1%的赖氨酸分枝二聚多肽溶液,取100μl加入步骤(1)的96孔板中,并快速混匀;
(3)置于37摄氏度,5%体积比的培养箱中培养24小时。同样条件下,将实施例2-4制备的赖氨酸分枝二聚肽替换赖氨酸分枝二聚肽1进行实验,结果表明,实施例1-4制备的赖氨酸分枝二聚肽均能形成水凝胶,在肉眼下为透明胶体。
3、锁水性能
取10mg实施例1制备的赖氨酸分枝二聚多肽1溶于1ml18.2mω·cm的纯净水中,可形成稳定水凝胶,其中多肽与水的质量比为1:99,因此是一种高效的锁水性物质。
同样条件下,实施例2-4制备的赖氨酸分枝二聚多肽替换赖氨酸分枝二聚肽1进行实验,结果表明,实施例1-4制备的赖氨酸分枝二聚肽均能形成稳定的水凝胶。
实施例6:赖氨酸分枝二聚肽对大鼠肝创伤出血以及股四头肌损伤出血的止血效果
1、供试品
由实施例1所得赖氨酸分枝二聚肽1
2、对照品
名称:氯化钠注射液
规格:250ml:2.25g
3、溶媒及供试品配制方法
溶媒名称:超纯水,现制现用
溶媒质量要求:取水时电阻率为18.2mω·cm
供试品溶液:精密称取供试品50mg,用移液器加入5ml超纯水,配制成质量浓度为1%的赖氨酸分枝二聚多肽溶液。
4、实验动物
大鼠,crl:cd(sd),spf级
体重范围:250-400g
周龄:约10-12周
来源:北京维通利华实验动物技术有限公司
5、动物实验方法
大鼠以3%戊巴比妥钠溶液(45mg/kg)腹腔注射麻醉。
肝脏创伤出血造模:腹部近剑突部位剃毛,消毒后用剪刀在手术区域切开腹部,暴露肝脏。用10号手术刀在肝脏左叶做一字型切口,切口长约1cm,深约0.5cm,造成肝脏创伤出血模型。
股四头肌损伤出血造模:大鼠右侧股四头肌剃毛,消毒后用剪刀在手术区域切开皮肤,分离皮肤和肌肉,暴露股四头肌(外侧头部分)。用10号手术刀沿股骨下缘在股四头肌上做一字型接口,切口长约2cm,深约1cm,切口以切破股静脉为限,造成股四头肌损伤出血模型。
给药:切开创口后,迅速将供试品溶液或氯化钠注射液均匀涂敷于创口处,用于创口出血控制。给药后,计时器记录完全止血时间。完全止血时间以静置状态下创口不再渗血为限。
本动物试验选择肝脏创伤出血模型和股四头肌出血模型作为供试品(由实施例1所得赖氨酸分枝二聚肽1)的止血效果探索,同时选用氯化钠注射液作为对照。试验结果表明,质量浓度为1%的赖氨酸分枝二聚多肽溶液在肝脏创伤出血模型和股四头肌出血模型中均有快速止血效果,完全止血时间均少于10秒,止血时间短。氯化钠注射液参照组出血时间均大于150秒。
同样条件下,将实施例1所得赖氨酸分枝二聚肽1分别替换为实施例2-4制备的赖氨酸分枝二聚肽,试验结果表明,质量浓度为1%的赖氨酸分枝二聚多肽溶液在肝脏创伤出血模型和股四头肌出血模型中均有快速止血效果,完全止血时间均少于10秒,止血时间短。氯化钠注射液参照组出血时间均大于150秒。
因此,本发明所述的赖氨酸分枝二聚多肽对创伤有快速止血功能,可制备成适合于临床使用的快速止血药物。
- 还没有人留言评论。精彩留言会获得点赞!