一种聚炔胺类化合物及其制备方法与流程
本发明属于有机化学的技术领域,涉及聚炔胺类化合物的合成,具体涉及一种聚炔胺类化合物及通过炔卤和磺酰胺反应制备该聚炔胺类化合物的方法。
背景技术:
发展新的聚合反应对于高分子材料科学来说是非常重要的。炔烃是易得或易合成的化学原料之一,利用炔烃构建功能性高分子具有重要的学术意义和技术意义,已经吸引了科学家们的广泛关注。炔胺的偶联聚合反应具有反应条件温和、反应效率高、原子经济等特点,符合绿色化学反应的定义,是一类新型的聚合反应。目前基于炔胺的小分子已经被广泛的报道,并作为有机产品、有机功能材料和生物活性化合物的中间体被广泛应用,又由于具有酰基基团的炔胺具有更高的稳定性,炔酰胺分子成为更有应用价值的合成中间体之一。
然而,炔胺的偶联聚合反应在有机领域却仍未被研究与报道,因此可以预见,开发简单、高效的聚炔胺合成途径将具有重要的科学意义和应用价值。
技术实现要素:
本发明的目的在于提供一种聚炔胺化合物的制备方法,该方法属于操作简便、反应高效、原子经济的绿色化学反应。
本发明的另一种目的在于提供利用上述方法得到的聚炔胺化合物,该化合物结构内具有三键,对于进一步反应作为中间体方面也将有重要应用。同时,该化合物易水解,在发展可降解材料等环境友好与绿色化学方面也极具潜力。
本发明的目的通过以下技术方案实现:
一种聚炔胺化合物的制备方法,包括以下步骤:
(1)在惰性气体保护下,在催化体系和有机溶剂中,将二元炔卤化合物和二元磺酰胺化合物混合,反应,冷却,得到反应母液;
(2)将反应母液加入沉淀剂中进行沉淀,收集沉淀物并干燥至恒重,得到聚炔胺化合物。
步骤(1)中所述二元炔卤化合物和二元磺酰胺化合物反应的摩尔比为1:1,二元炔卤化合物在有机溶剂中的浓度为0.1-0.2mol/L。
步骤(1)中所述催化体系为含有CuSO4·5H2O,K2CO3和1,10-邻菲罗啉的体系;
所述CuSO4·5H2O的用量为二元炔卤化合物用量的10-20mol%,1,10-邻菲罗啉的用量为二元炔卤化合物用量的20-40mol%,K2CO3在有机溶剂中的浓度为0.2-0.4mol/L。
所述有机溶剂为二甲基亚砜(DMSO)或N,N-二甲基甲酰胺(DMF)中的一种。
步骤(1)中所述反应的温度为50-100℃,反应的时间为24-48h;
步骤(2)中沉淀剂为甲醇。
步骤(2)中所述反应母液加入沉淀剂中的方式为滴加(滴加的速度为1~3滴/秒),且将反应母液加入沉淀剂中之前先用四氢呋喃进行稀释,稀释过后进行过滤。
步骤(1)中所述的二元炔卤化合物的结构式为:其中X为氯原子或溴原子;R选自以下16-26中的任意一种,并且不限于以下16-26种;其中R1与R2相同或者不同,R1为亚烷基(-CnH2n-,n为整数)、亚烷氧基(-CnH2nO-,n为整数)、氧(O)、亚苯基、亚烷基中一个或多个C被苯基取代(取代的碳数小于亚烷基中碳数)、亚烷氧基中一个或多个C被苯基和/或氧取代(取代的碳数小于亚烷基中碳数);R2为亚烷基(-CnH2n-,n为整数)、亚烷氧基(-CnH2nO-,n为整数)、氧(O)、亚苯基、亚烷基中一个或多个C被苯基取代(取代的碳数小于亚烷基中碳数)、亚烷氧基中一个或多个C被苯基和/或氧取代(取代的碳数小于亚烷基中碳数);*为连接处;
所述的二元磺酰胺化合物选自以下1-15中的任意一种,并且不限于以下15种:其中R1为亚烷基(-CnH2n-,n为整数)、亚烷氧基(-CnH2nO-,n为整数)、氧(O)、亚苯基、亚烷基中一个或多个C被苯基取代(取代的碳数小于亚烷基中碳数)、亚烷氧基中一个或多个C被苯基和/或氧取代(取代的碳数小于亚烷基中碳数);R2为烷基、烷氧基、苯基、烷基取代的苯基、烷氧基取代的苯基、烷基中一个或多个C被苯基取代(取代的碳数小于烷基中碳数)、烷氧基中一个或多个C被苯基和/或氧取代(取代的碳数小于亚烷基中碳数);
本发明还提供了一种聚炔胺化合物,由上述方法制备得到。
所述聚炔胺化合物的结构为其中,R1、R1′与R2是由上述二元炔卤化合物和二元磺酰胺化合物反应脱除卤化氢后原结构中对应的基团,n为2-200之间的整数。
该聚炔胺化合物结构内仍留有三键,对于进一步反应作为中间体方面也将有重要应用。同时,该化合物易水解,在发展可降解材料等环境友好与绿色化学方面也极具潜力。
与现有技术相比,本发明具有如下优点:
1、本发明使用炔卤和磺酰胺聚合得到聚炔胺,据我们所知,该类聚合反应从未被报道,因此具有很高的科研价值、应用价值以及很好的发展前景;
2、本发明的制备方法工艺简单,使用的催化剂和原料易得,可通过购买或简单的实验操作得到;
3、本发明的制备方法反应条件温和、高效、节约能源,并且无副产物生成,具有原子经济性的特点;
4、本发明的制备方法基团耐受性较强,可在单体中引入多种功能性基团;
5、通过本发明的制备方法得到的聚炔胺化合物易水解,在可降解材料等环境友好化学与绿色化学方面极具应用前景。
附图说明
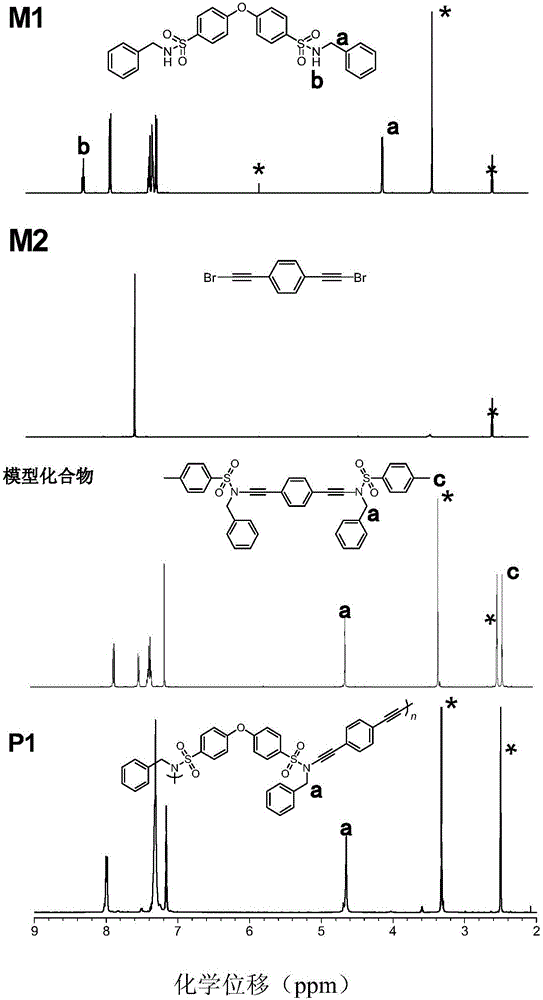
图1为本发明实施例1制备的聚炔胺化合物(P1)及其相应单体(M1、M2)以及模型化合物在氘代DMSO中核磁共振氢谱对比图;
图2为本发明实施例1制备的聚炔胺化合物(P1)及其相应单体(M1、M2)以及模型化合物在氘代DMSO中核磁共振碳谱对比图;
图3为本发明实施例1制备的聚炔胺化合物(P1)及其相应单体(M1、M2)以及模型化合物的红外吸收光谱图;
图4为本发明实施例4制备的聚炔胺类化合物P2在不同水含量下的荧光发射光谱;
图5为本发明实施例4制备的聚炔胺类化合物P2在不同水含量下的量子产率图。
具体实施方式
下面结合实施例和附图对本发明进行具体地描述,但本发明的保护范围不限于以下实施例。
实施例1
一种聚炔胺化合物P1,其结构式如下:
所述聚炔胺化合物通过炔卤与磺酰胺单体反应制备得到,其具体反应方程式如式(一):
(1)单体M1的合成方法为:在0℃下,往250mL两口瓶中加入9.0mmol(3.29g)磺酰氯,抽真空换N2后加入150mL二氯甲烷与36.9mmol(4.03mL)苄胺,将反应体系在常温下搅拌2小时后,用二氯甲烷和水萃取三次、旋干,粗产物用硅胶色谱柱进行分离纯化并在40℃温度下真空干燥,得到7.7mmol(3.90g)产物(单体M1),产率为85%;图1的核磁图中M1单体的8.20为-NH峰,4.04为-CH2峰,其中,3.32为水峰,2.50为DMSO-d6峰;图3中单体M1存在-NH峰;
(2)单体M2的合成方法为:在250mL单口瓶中加入10.0mmol(1.26g)1,4-二乙炔基苯、22.0mmol(3.89g)NBS、2.0mmol(0.34g)硝酸银,再加入100mL丙酮后,将体系在常温下搅拌3小时,随后过滤、旋干,粗产物用硅胶色谱柱进行分离纯化,在40℃温度下真空干燥后,得到7.8mmol(2.20g)产物(单体M2),产率为78%;图1的核磁图中M2单体的7.48处为苯环上的H峰,其中,3.32为水峰,2.50为DMSO-d6峰;图3中存在碳碳三键峰;
(3)所述的聚炔胺类化合物的制备步骤为:在10mL聚合管中依次加入0.2mmol(0.11g)单体M1、0.2mmol(0.06g)单体M2、0.03mmol(0.005g)CuSO4·5H2O、0.06mmol(0.01g)、1,10-邻菲罗啉、0.6mmol(0.08g)K2CO3,抽真空换N2后加入2mL DMSO,将体系升温至65℃后以400转每分钟的速率搅拌24小时;反应结束后用2mL四氢呋喃稀释反应体系,使体系过滤掉硫酸铜后滴加到沉淀剂无水甲醇中进行沉降,静置12小时、过滤、真空干燥后在40℃温度下真空干燥,得到0.12g聚合物P1,产率为86%,分子量达到18000g/mol;图1的核磁图中的P1图可以看到,单体M1的-NH峰已经消失,而-CH2从4.04位移到4.65,其中,3.32为水峰,2.50为DMSO-d6峰;图3中可观测到的反应过后P1中-NH的消失,碳碳三键峰的存在;
(4)模型化合物具体反应方程式如下:
该模型化合物的制备步骤为:在50mL双口瓶中依次加入2.0mmol(0.57g)底物1、4.2mmol(1.10g)底物2、0.4mmol(0.10g)CuSO4·5H2O、0.8mmol(0.14)、1,10-邻菲罗啉、8.0mmol(1.11g)K2CO3,抽真空换N2后加入10mL DMSO,将体系升温至65℃后以400转每分钟的速率搅拌36小时,反应结束后用二氯甲烷和水萃取三次、旋干,粗产物用硅胶色谱柱进行分离纯化并在40℃温度下真空干燥,得到1.8mmol(1.16g)产物,产率为90%。
本实施例制备的聚炔胺化合物(P1)及其相应单体(M1、M2)以及模型化合物在氘代DMSO中核磁共振氢谱如图1所示,在氘代DMSO中核磁共振碳谱如图2所示,红外吸收光谱图如图3所示。
实施例2
本实施例将实施例1中反应时间改为80℃,其他制备条件与实施例1的制备方法相同,得到聚合物0.13g,产率为90%,分子量达到17000g/mol。
实施例3
本实施例将实施例1中的CuSO4·5H2O投料改为0.04mmol(0.007g),1,10-邻菲罗啉投料改为0.08mmol(0.02g),K2CO3投料改为0.80mmol(0.11g),其他制备条件与实施例1的制备方法相同,得到聚合物0.12g,产率为81%,分子量达到18000g/mol。
实施例4
一种聚炔胺化合物P2,其结构式所示:
所述聚炔胺化合物通过炔卤与磺酰胺单体反应制备得到,其具体反应方程式如式(二):
(1)单体M1的合成方法同实例1所述;
(2)单体M3的合成方法如下所述:在250mL单口瓶中加入3.0mmol(1.14g)二乙炔基四苯基乙烯、6.6mmol(1.17g)NBS、0.6mmol(0.10g)硝酸银,再加入60mL丙酮后,将体系在常温下搅拌3小时,随后过滤、旋干,粗产物用硅胶色谱柱进行分离纯化,在40℃温度下真空干燥后得到2.7mmol(1.45g)产物,产率为90%;
本步骤中的二乙炔基四苯基乙烯按照文献[Hu,R.;Lam,J.W.Y.;Liu,J.;Sung,H.H.Y.;Williams,I.D.;Yue,Z.;Wong,K.S.;Yuen,M.M.F.;Tang,B.Z.,Hyperbranched conjugated poly(tetraphenylethene):synthesis,aggregation-induced emission,fluorescent photopatterning,optical limiting and explosive detection.Polymer Chemistry 2012,3(6),1481-1489.]公开的方法制备;
(3)所述的聚炔胺类化合物的制备步骤如下:在10mL聚合管中依次加入0.2mmol(0.10g)单体M1、0.2mmol(0.11g)单体M3、0.03mmol(0.005g)CuSO4·5H2O、0.06mmol(0.01g)、1,10-邻菲罗啉、0.6mmol(0.08g)K2CO3,抽真空换N2后加入2mL DMSO,将体系升温至65℃后以400转每分钟的速率搅拌24小时;反应结束后用2mL四氢呋喃稀释反应体系,使体系过滤掉硫酸铜后滴加到沉淀剂无水甲醇中进行沉降,静置12小时、过滤、真空干燥后在40℃温度下真空干燥,得到0.15g聚合物P2,产率为86%,分子量达到11000g/mol。
该方法得到的聚合物具有特殊的光电性质,图4为该聚合物P2在不同水含量下的荧光发射光谱。随着含水量的升高,该聚合物溶液的发光逐渐增强,其中,当水含量为95%时,该聚合物在该溶液下具有最高的发光效率。图5为聚合物P2在不同水含量下的量子产率图(激发波长为340nm),在含水量为95%时,有最高量子产率24.7%。
实施例5
一种聚炔胺化合物P3,其结构式所示:
所述聚炔胺化合物通过炔卤与磺酰胺单体反应制备得到,其具体反应方程式如式(三):
(1)单体M4的合成方法为:在0℃下,往250mL两口瓶中加入9.0mmol(3.29g)磺酰氯,抽真空换N2后加入150mL二氯甲烷与36.9mmol(2.05mL)乙胺,将反应体系在常温下搅拌2小时后,用二氯甲烷和水萃取三次、旋干,粗产物用硅胶色谱柱进行分离纯化并在40℃温度下真空干燥,得到8.1mmol(3.11g)产物(单体M4),产率为90%;
(2)单体M5的合成方法为:
(2-1)在250mL两口瓶中加入15.0mmol(3.43g)双酚A、45mmol(6.22g)碳酸钾和33.0mmol(8.25g)对溴溴苄,接着往反应体系加入100mL丙酮,加热回流反应12小时后,冷却,用去离子水反复清洗白色沉淀物,干燥后得到7.64g白色固体产物1,产率为90%;
(2-2)在250mL两口瓶中加入10.0mmol(5.66g)白色固体1、0.5mmol(0.35g)双三苯基磷二氯化钯、0.5mmol(0.10g)碘化亚铜、0.5mmol(0.13g)三苯基膦,并抽真空充氮气三次,接着向反应体系加入100mL经过氮气鼓泡处理的三乙胺和20mL重蒸过的四氢呋喃,再往体系中加入4mL(30.0mmol)三甲基硅乙炔,加热至90℃反应24小时后,冷却,用100mL饱和氯化铵溶液淬灭反应,过滤,滤液用二氯甲烷萃取三次,将有机相合并浓缩,得到的粗产物用硅胶色谱柱进行分离,淋洗剂为石油醚,得到5.40g白色固体产物2,产率为90%;
(2-3)在250mL单口瓶中加入5.0mmol(3.00g)白色固体2和25.0mmol(1.40g)氢氧化钾,再往里加入25mL甲醇、25mL四氢呋喃、5mL去离子水,室温下搅拌12小时后,反应混合液用二氯甲烷萃取三次,将有机相合并浓缩,得到的粗产物用硅胶色谱柱进行分离,淋洗剂为石油醚,得到2.17g白色固体产物3,产率为95%;
(2-4)在250mL单口瓶中加入2.5mmol(1.14g)白色固体3、5.5mmol(0.98g)NBS、0.5mmol(0.08g)硝酸银,再加入60mL丙酮后,将体系在常温下搅拌3小时,随后过滤、旋干,粗产物用硅胶色谱柱进行分离纯化,在40℃温度下真空干燥后得到1.38g产物,即为单体M5,产率为90%;
(3)所述的聚炔胺类化合物的制备步骤为:在10mL聚合管中依次加入0.2mmol(0.08g)单体M4、0.2mmol(0.12g)单体M5、0.03mmol(0.005g)CuSO4·5H2O、0.06mmol(0.01g)、1,10-邻菲罗啉、0.6mmol(0.08g)K2CO3,抽真空换N2后加入2mL DMSO,将体系升温至65℃后以400转每分钟的速率搅拌24小时;反应结束后用2mL四氢呋喃稀释反应体系,使体系过滤掉硫酸铜后滴加到沉淀剂无水甲醇中进行沉降,静置12小时、过滤、在40℃温度下真空干燥后得到0.13g聚合物P3,产率为78%。
本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!